يحدث التوازن الديناميكي أو التوازن الكيميائي للتفاعل عندما تحدث التفاعلات الأمامية والعكسية في وقت واحد. يتم تمثيل هذه الأنظمة القابلة للعكس المزعومة بأسهم في كلا الاتجاهين:  أو
أو  . تم ذكر مثال للتفاعل القابل للانعكاس في الصورة أعلاه ، بين غاز اليود وغاز الهيدروجين.
. تم ذكر مثال للتفاعل القابل للانعكاس في الصورة أعلاه ، بين غاز اليود وغاز الهيدروجين.
في بداية التفاعل ، تكون كمية المواد المتفاعلة هي القصوى وكمية المنتجات صفر. ومع ذلك ، تتفاعل المواد المتفاعلة مع بعضها البعض ، مما يقلل من تركيزها ويزيد من تركيز المنتجات المشكلة. كما أن معدل تطور التفاعل المباشر آخذ في التناقص.
مع زيادة تركيز المنتجات ، يبدأ التفاعل العكسي وتتشكل المواد المتفاعلة مرة أخرى ؛ يزيد معدل تطور التفاعل العكسي أيضًا.
عند الوصول إلى التوازن الكيميائي ، عند درجة حرارة ثابتة ، تكون معدلات تطور التفاعلات الأمامية والعكسية متساوية.
الجميعمباشرة = الكل معكوس
المعدلات هي نفسها ، لكن التركيزات ليست كذلك. من غير المحتمل أن تكون تركيزات الكواشف والمنتجات هي نفسها. فقط في حالات نادرة يحدث هذا. في معظم الحالات يكون تركيز الكواشف أعلى من تركيز المنتجات أو العكس.
وهكذا ، لدينا ثلاث طرق ممكنة لتمثيل معدلات التنمية بيانيا التفاعلات العكسية والمباشرة المتعلقة بتركيزات المواد المتفاعلة والمنتجات فوق زمن. لنلق نظرة على كل حالة:
الحالة الأولى: تركيزات متساوية:
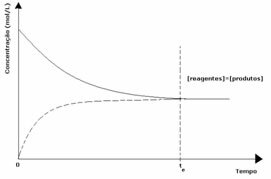
كما هو موضح في الرسم البياني ، في الوقت tو التفاعلات الأمامية والعكسية هي نفسها ، وفي هذه الحالة تكون تركيزات المواد المتفاعلة والمنتجات متماثلة. وبالتالي ، لا يتم تحويل التوازن إلى أي جانب ، فإن شدة كلا التفاعلين هي نفسها ، كما هو موضح أدناه:
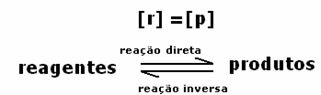
الحالة الثانية: تركيز الكواشف أكبر من تركيز المنتجات:
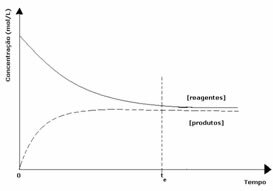
في هذه الحالة ، لوحظ أنه عند الوصول إلى التوازن ، يكون تركيز المواد المتفاعلة أكبر من تركيز المنتجات. وهكذا ، استنتج أنه إذا كان هناك تفاعل أكثر ، فإن التفاعل العكسي يحدث بكثافة أكبر. رد الفعل ينتقل إلى اليسار:
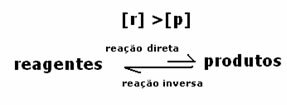
الحالة الثالثة: تركيز المنتجات أكبر من تركيز الكواشف:
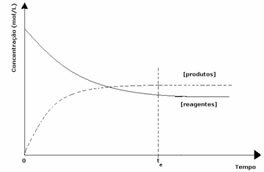
نظرًا لأن تركيز المنتجات عند التوازن أكبر ، فهذا يعني أن التفاعل يكون إلى اليمين ، لأن التفاعل المباشر (مع تكوين المنتجات) يحدث بدرجة أكبر الشدة.
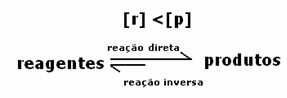
ما سيشير إلى ما إذا كان التفاعل يميل إلى اليمين أو اليسار سيكون ثابت التوازن K ، والذي يعتمد فقط على درجة الحرارة.
بقلم جينيفر فوغاسا
تخرج في الكيمياء
فريق مدرسة البرازيل
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/estudo-grafico-equilibrio-quimico.htm

