تعلم كيفية تطبيق القانون الأول للديناميكا الحرارية في مواقف مختلفة ، وحل التمارين واختبر معلوماتك من خلال تمارين محلولة ومفسرة.
السؤال رقم 1
ينص القانون الأول للديناميكا الحرارية على ما يلي:
أ) لا يمكن إنشاء الطاقة أو إتلافها ، ولكن يمكن تحويلها من شكل إلى آخر.
ب) يتم الحفاظ على الطاقة دائمًا ، ولكن لا يمكن تحويلها من شكل إلى آخر.
ج) يمكن إنشاء الطاقة أو إتلافها ، لكن لا يمكن تحويلها من شكل إلى آخر.
د) لا يمكن الحفاظ على الطاقة ، ولكن يمكن تحويلها من شكل إلى آخر.
القانون الأول للديناميكا الحرارية هو مبدأ الحفاظ على الطاقة ، لذلك في النظام عند الإغلاق ، تظل كمية الطاقة ثابتة ولا يمكن تحويلها إلا من شكل إلى آخر. آخر.
السؤال 2
افترض أن نظامًا مغلقًا يتلقى 100 J من الحرارة أثناء القيام بشغل 50 J. ما هو التغير في الطاقة الداخلية للنظام؟
أ) -50 جول
ب) 0 ي
ج) 50 جول
د) 100J
هـ) 150J
فحص العلامات:
الحرارة المستلمة موجبة Q > 0.
العمل المنجز موجب W > 0.
وفقًا للقانون الأول لدينا:
السؤال 3
يتبادل نظام الغاز المثالي 500 جول من الحرارة مع البيئة الخارجية. بافتراض أن هذه العملية هي تبريد متساوي القياس ، حدد العمل والطاقة الداخلية ، على التوالي.
أ) 500 J و 0 J
ب) - 500 و 0 ي
ج) 0 J و 500 J
د) 0 جول و - 500 جول
هـ) -500 جول و 500 جول
نظرًا لأن العملية متساوية القياس ، فلا يوجد تغيير في الحجم ، وبالتالي يكون الشغل صفرًا.
وفقًا للقانون الأول للديناميكا الحرارية:
نظرًا لأنه تبريد ، فإن النظام يفقد الحرارة ، لذلك:
السؤال 4
يتم ضغط 8 مولات من الغاز المثالي في نظام أسطوانة مكبس بعمل 1000 J من الشغل. أثناء العملية ، يتم فقد 400 J من الحرارة في البيئة الخارجية. طاقته الداخلية والتغير في درجة حرارته متساويان على التوالي
المعطى: R = 8.31 جول / مول. ك
أ) - 1400 J والاختلاف التقريبي 6 ك
ب) 600 J والاختلاف التقريبي 6 ك
ج) 600 J والاختلاف التقريبي 14 ك
د) - 1400 J والاختلاف التقريبي 14 ك
الطاقة الداخلية
عندما يتلقى النظام العمل ، تكون علامته سلبية ، وكذلك الحرارة التي يتم فقدها في هذه العملية.
القانون الأول للديناميكا الحرارية هو:
باستبدال القيم ، نحصل على:
R = 8.31 جول / مول ك
درجة حرارة
بموجب قانون جول ، لدينا:
السؤال 5
يخضع الغاز المثالي للضغط ، حيث يؤدي 500 J من الشغل. في نهاية هذا التحول ، تغيرت الطاقة الداخلية للنظام 200 J أقل مما كانت عليه في البداية. كانت كمية الحرارة التي يتبادلها الغاز
أ) - 700 جول
ب) - 300 جول
ج) 300J
د) 0J
ه) 700 جول
منذ استلام العمل ، أي عمل مقاوم ، تكون علامته سلبية.
استبدال القيم في معادلة القانون الأول للديناميكا الحرارية:
السؤال 6
(CEDERJ 2021) في إحدى مراحل الدورة التي يتم تنفيذها بواسطة غاز مثالي في مكيف الهواء ، يتم زيادة ضغط الغاز مع الحفاظ على ثبات حجمه. في هذه المرحلة من الدورة ، يكون الشغل W الذي يقوم به الغاز ، وكمية الحرارة Q التي يمتصها والتغير ΔT في درجة حرارته ، على التوالي:
أ) W < 0 و Q 0 و T < 0
ب) W = 0 ، Q 0 و ΔT > 0
ج) W = 0 ، Q = 0 و T = 0
د) W > 0 و Q 0 و T > 0
بيانات:
يزيد الضغط P ؛
يظل الحجم ثابتًا ؛
عمل
بما أن الحجم ثابت ، فإن الشغل W يساوي صفرًا.
يذهب القانون الأول للديناميكا الحرارية على النحو التالي:
نظرًا لأن الحرارة موجبة ، سيكون التغيير في الطاقة الداخلية إيجابيًا أيضًا.
حرارة
منذ امتصاص الحرارة ، فهي إيجابية.
درجة حرارة
بموجب قانون الغاز:
أين،
ن هو عدد الشامات
R هو ثابت الغاز العالمي
وبالتالي ، فإن درجة الحرارة تعتمد فقط على الضغط ، لأن الحجم ثابت ، ويكون موجبًا.
السؤال 7
(UNICENTRO 2018) وفقًا للقانون الأول للديناميكا الحرارية ، يكون التغيير في الطاقة الداخلية للنظام ، ΔU ، هو يُعطى بالفرق بين الحرارة المتبادلة مع البيئة الخارجية ، Q ، والعمل ، W ، المنجز في العملية الديناميكا الحرارية. بالنظر إلى هذه المعلومات ، إذا تمدد غاز أحادي الذرة ليبقى دائمًا عند نفس درجة الحرارة ، يمكن تمثيل هذا التحول بالمعادلة
أ) ΔU + W = 0
ب) ΔU - W = 0
ج) س - ث = 0
د) س + ΔU = 0
تحدث عملية متساوي الحرارة دون تغيير في درجة الحرارة.
ترتبط الطاقة بدرجة الحرارة من خلال:
حيث n هو عدد المولات و R هو ثابت الغاز العام. نظرًا لأن n و R ثابتان ، فلا يوجد سوى اختلاف في درجة الحرارة ، و
يذهب القانون الأول للديناميكا الحرارية على النحو التالي:
السؤال 8
(URCA 2016) وفقًا للقانون الأول للديناميكا الحرارية ، إذا تم إطلاق الغاز أثناء عملية متساوية الحرارة يمر بها غاز مثالي ذي كتلة ثابتة كمية حرارة مقدارها 50 كالوري ثم التغير في الطاقة الداخلية والعمل الذي يقوم به الغاز في هذه العملية ، على التوالى:
أ) 0 و 50 كالوري.
ب) 50 كالوري و 0.
ج) 0 و 0.
د) 50 كالوري و -50 كالوري.
ه) 0 و -50 كال.
يرتبط التغيير في الطاقة الداخلية ارتباطًا مباشرًا بالتغير في درجة الحرارة. نظرًا لأن العملية متساوية الحرارة ، فلا يوجد تغيير في درجة الحرارة ، لذلك .
من القانون الأول للديناميكا الحرارية:
منذ إطلاق الحرارة ، فإن علامتها سلبية.
السؤال 9
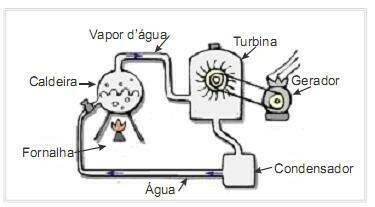
(UFRN 2012) تعد الكتلة الحيوية أحد المصادر الرئيسية للطاقة المتجددة ، وبالتالي فإن الآلات التي تستخدمها كوقود لتوليد الطاقة مهمة من وجهة نظر بيئية. مثال شائع جدًا هو استخدام الكتلة الحيوية لتشغيل التوربينات البخارية لتوليد العمل. يوضح الشكل الموجود على الجانب بشكل تخطيطي محطة طاقة حرارية مبسطة.
في هذا المصنع الكهروحراري ، ينتج عن حرق الكتلة الحيوية في الفرن حرارة ، مما يؤدي إلى تسخين الماء في الغلاية وتوليد بخار عالي الضغط. يتم تمرير البخار بدوره من خلال الأنابيب إلى التوربين الذي ، تحت تأثيره ، يبدأ في تحويل ريشه.
افترض أن فقد الحرارة بسبب الاختلافات في درجة الحرارة بين أجزاء المحرك الحراري والبيئة لا يكاد يذكر. في هذا السياق ، الاختلاف في الطاقة الداخلية لمياه الغلايات
أ) أكبر من مجموع الحرارة التي يتم توفيرها لها عن طريق حرق الكتلة الحيوية والعمل المنجز على التوربين.
ب) يساوي مجموع الحرارة الموردة لها عن طريق حرق الكتلة الحيوية مع الشغل المنجز على التوربين.
ج) يساوي الفرق بين الحرارة التي يتم توفيرها لها عن طريق حرق الكتلة الحيوية والعمل المنجز على التوربين.
د) أكبر من الفرق بين الحرارة التي يتم توفيرها لها عن طريق حرق الكتلة الحيوية والعمل المنجز على التوربين.
يتلقى الماء الموجود في الغلاية طاقة على شكل حرارة من حرق الوقود ويطلق طاقة على شكل عمل يتم إجراؤه على التوربين.
السؤال 10
(UECE 2021) فيما يتعلق بخصائص الغازات ، انتبه إلى العبارات التالية:
أنا. بالنسبة للغاز المثالي ، فإن الطاقة الداخلية هي دالة للضغط فقط.
ثانيًا. الحرارة التي يمتصها الغاز عند تغيير حالته مستقلة عن العملية.
ثالثا. الطاقة الداخلية للغاز المثالي هي دالة لدرجة الحرارة فقط وهي مستقلة عن العملية.
رابعا. في تمدد متساوي الحرارة لغاز مثالي ، فإن الشغل الذي يقوم به يكون مساويًا للحرارة الممتصة.
وصحيح ما ورد فيه فقط
أ) الأول والثاني.
ب) الثالث والرابع.
ج) الأول والرابع.
د) الثاني والثالث.
ثالثا. صحيح. الطاقة الداخلية للغاز المثالي هي دالة لدرجة الحرارة فقط وهي مستقلة عن العملية.
يرتبط التغيير في الطاقة الداخلية ارتباطًا مباشرًا بالتغير في درجة الحرارة.
حيث n هو عدد المولات و R هو ثابت الغاز المثالي ، كونه ثوابت ، فإن درجة الحرارة فقط هي التي تحدد الطاقة الداخلية للغاز.
رابعا. صحيح. في تمدد متساوي الحرارة لغاز مثالي ، فإن الشغل الذي يقوم به يكون مساويًا للحرارة الممتصة.
نظرًا لأنه متساوي الحرارة ، فلا يوجد أي تغيير في درجة الحرارة ، وبالتالي فإن التغيير في الطاقة الداخلية هو صفر. حسب القانون الأول للديناميكا الحرارية:
تعلم المزيد مع:
- القانون الأول للديناميكا الحرارية
- الديناميكا الحرارية: القوانين والمفاهيم والصيغ والتمارين
- تمارين في الديناميكا الحرارية
- قانون الغاز
ASTH ، رافائيل. تمارين القانون الأول للديناميكا الحرارية.جميع المواد, [اختصار الثاني.]. متوفر في: https://www.todamateria.com.br/exercicios-da-primeira-lei-da-termodinamica/. الوصول إلى:
نرى أيضا
- تمارين في الديناميكا الحرارية
- الديناميكا الحرارية
- تحول ثابت الحرارة
- تمارين في الكيمياء الحرارية
- القانون الأول للديناميكا الحرارية
- العلوم الطبيعية وتقنياتها: العدو
- طاقة حرارية
- القانون الثاني للديناميكا الحرارية