ا كلوريد الفينيل إنها الهيدروكربون مكلور سام ومسرطن. إنه غاز عديم اللون في درجة حرارة الغرفة ، وهو سريع الاشتعال وحساس للحرارة.
هو المونومر المستخدم في تصنيع البولي فينيل كلوريد ، وهي مادة تعرف باسم PVC. ا PVC هو لدن حراري مقاوم للحرارة (على عكس المونومر الخاص به) وله العديد من التطبيقات في الحياة اليومية ، مثل طلاء الأسلاك الكهربائية ، وبناء الأنابيب وأنواع مختلفة من التعبئة والتغليف.
اقرأ أيضا:الأسبستوس - ألياف طبيعية ذات تطبيقات صناعية واسعة ، لكنها شديدة السمية للإنسان
مواضيع هذا المقال
- 1 - ملخص عن كلوريد الفينيل
- 2 - خواص كلوريد الفينيل
- 3 - ما هو كلوريد الفينيل؟
- 4 - خواص كلوريد الفينيل
- 5 - ما هو استخدام كلوريد الفينيل؟
- 6 - الحصول على كلوريد الفينيل
-
7 - احتياطات مع كلوريد الفينيل
- كلوريد الفينيل والسرطان
- 8 - حدوث كلوريد الفينيل
- 9 - تاريخ كلوريد الفينيل
ملخص عن كلوريد الفينيل
كلوريد الفينيل هو هيدروكربون مكلور بالصيغة H2C = CHCl.
إنها غاز عديم اللون ورائحة حلوة وقابل للاشتعال.
كلوريد الفينيل غير مستقر حرارة، يخضع للتحلل.
التطبيق الرئيسي لكلوريد الفينيل في تصنيع البولي فينيل كلوريد (PVC).
PVC عبارة عن لدائن حرارية لها العديد من التطبيقات ، مثل الأنابيب ، والأجزاء ، والطلاء ، والتغليف ، إلخ.
كلوريد الفينيل سام وله تأثير مسرطن.
خصائص كلوريد الفينيل
الصيغة الجزيئية: CH2CHCl (سي2ح3Cl).
الكتلة الجزيئية: 62.498 جم / مول.
الحالة الفيزيائية: غاز (عديم اللون ورائحة قوية).
كثافة: 0.91 جم / مل.
الذوبان في الماء: قليل الذوبان (0.6 جم في 100 مل من الماء ، 20 درجة مئوية).
درجة حرارة الانصهار: -154 درجة مئوية.
درجة حرارة الغليان: -13 درجة مئوية.
لا تتوقف الان... هناك المزيد بعد الدعاية ؛)
ما هو كلوريد الفينيل؟
كلوريد الفينيل هو هيدروكربون مكلور بالصيغة H2C = CHCl. في درجة حرارة الغرفة ، يحدث مع a غاز عديم اللون وسريع الاشتعال.
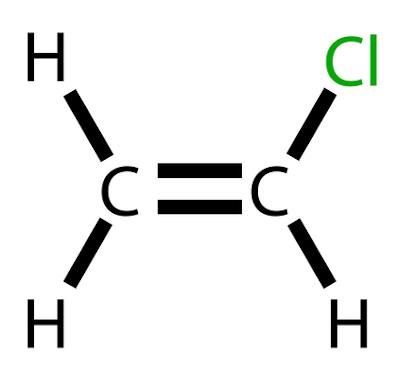
كلوريد الفينيل ، ويسمى أيضًا كلورو إيثين أو مونومر كلوريد الفينيل ، هو أ منتج كيميائي ذو أهمية كبيرة في صناعة، لها تطبيقات خاصة في تصنيع بوليمر كلوريد البوليفينيل ، المعروف باسم PVC. يحتل هذا المركب قائمة المنتجات العشرين المشتقة منها البترول ذات أهمية صناعية واقتصادية أكبر.
اقرأ أيضا:البنزوبيرين - الهيدروكربونات المسرطنة الموجودة في دخان السجائر واللحوم المشوية
ملامح كلوريد الفينيل
كلوريد الفينيل هو أ غاز عديم اللون ذو رائحة خفيفة وحلوة. لها خاصية كونها شديدة الاشتعال.
عند التعرض لمصادر الحرارة ، قد تتعرض للتحلل وتنبعث منها أبخرة سامة في ثاني أكسيد الكربون, أول أكسيد الكربونوكلوريد الهيدروجين والفوسجين. لأنه مركب عضوي ، فإن قابليته للذوبان في الماء منخفضة للغاية ، ومن ناحية أخرى قابل للذوبان في مواد مثل الإيثانول, البنزين ورابع كلوريد الكربون.
في وجود الرطوبة ، يصبح كلوريد الفينيل مادة أكالة ويمكن أن يهاجم حديد و ال فُولاَذ. لديها القدرة على البلمرة عند تعرضها للحرارة في الهواء الجوي ، من خلال تفاعل طارد للحرارة. تستمد هذه الملكية العديد من تطبيقاتها الصناعية.
يتطلب كلوريد الفينيل الاهتمام بسبب أنها سامة ومسببة للسرطان.
ما هو كلوريد الفينيل المستخدم؟
كلوريد الفينيل هو مونومر يستخدم لتصنيع بوليمر بولي كلوريد الفينيل (بولي فينيل كلوريد) ومذيبات مكلورة أخرى.
PVC عبارة عن لدن حراري يستخدم في صناعة التعبئة والتغليف والأحذية والتوصيلات الكهربائية والكابلات ، الأنابيب والنوافذ والأنابيب وأكياس جمع الدم والملابس ، من بين أشياء أخرى لا حصر لها أغراض.

ا يتكون PVC من بلمرة كلوريد الفينيل. في هذه العملية الكيميائية ، يضيف عدد كبير من جزيئات كلوريد الفينيل مع بعضها البعض ، مما يشكل بنية كيميائية كبيرة.
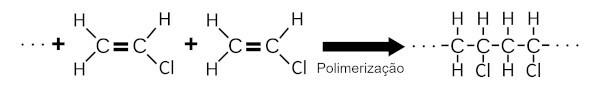
ا مادة PVC مقاومة للهب ولهذا السبب يتم استخدامه على نطاق واسع في طلاء الأسلاك والكابلات الكهربائية والطلاء السكني.
على الرغم من أن كلوريد الفينيل مركب كيميائي يتطلب الانتباه بسبب سميته و عدم الاستقرار الحراري ، بوليمر PVC مستقر جدًا لمصادر الحرارة ، وهو غير سام ويمكن تخزينه بأمان.
حتى عام 1974 ، كان كلوريد الفينيل يستخدم في الهباء الجوي. في الماضي ، كان يستخدم كمخدر استنشاق. مع معرفة سمية هذا المركب ، تم إيقاف هذه التطبيقات.
الحصول على كلوريد الفينيل
تركيب كلوريد الفينيل المستخدم على نطاق صناعي هو يبدأ بمركب الإيثيلين أو الإيثين (CH2= CH2) ويمكن أن تحدث بطريقتين.
في الحالة الأولى ، يتم تحويل الإيثيلين إلى 1،2 ثنائي كلورو إيثان من خلال التفاعل مع غاز الكلور. بعد ذلك ، عن طريق تسخين 1،2-ثنائي كلورو إيثان في وجود محفز ، يتم الحصول على كلوريد الفينيل كمنتج رئيسي و حامض الهيدروكلوريك كمنتج ثانوي.
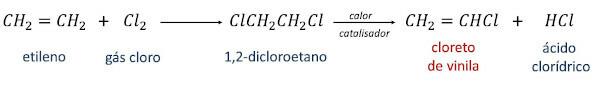
في مسار التفاعل الثاني ، المعروف باسم الكلورة المؤكسدة ، يكون التفاعل بين الإيثيلين وحمض الهيدروكلوريك و الأكسجين من الغلاف الجوي نفسه ، في ظل وجود حرارة ومحفز ، يولد كلوريد الفينيل والماء كمنتجات.

عادة ، يتم بناء مركز تصنيع كلوريد الفينيل لاستيعاب عمليتي التصنيع. تم الاستشهاد به ، بحيث يعمل حمض الهيدروكلوريك المتولد في الطريقة الأولى ككاشف لتنفيذ الطريقة الثانية طريق.
احتياطات مع كلوريد الفينيل
كلوريد الفينيل مركب سام. لأنه غاز ، الشكل الرئيسي للتلوث هو الاستنشاق.ولهذا السبب يجب أن يتم التعامل معها دائمًا باستخدام المعدات المناسبة ، مثل الأقنعة الواقية من الغازات.
التعرض لهذه المادة يؤثر على الجهاز العصبي المحيطية والمركزية ، مما تسبب في تلف الكبد. أ يمكن أن يؤدي التعرض المستمر إلى ظاهرة رينود، وهي مجموعة من الأعراض التي تشمل آلام المفاصل والعضلات وتغيرات الجلد ، والتي يمكن أن تتطور إلى فقدان كامل لمرونة الجلد ، حتى أنها تؤثر على الأعضاء الأعضاء الداخلية والأوعية الدموية.
وتشمل الآثار الأخرى النشوة والارتباك والإجهاض والعيوب الخلقية. كما يتم تسجيل إصابات أنسجة العين.
تعتمد الأعراض على مستوى التعرض للمادة ، وتتراوح بين الدوخة والغثيان والاضطرابات البصرية والصداع والرنح عند التعرض الحاد (من 1000 إلى 8000 جزء في المليون من كلوريد الفينيل في الهواء) للتأثير المخدر وعدم انتظام ضربات القلب والفشل التنفسي المميت في حالات التعرض لمستويات أعلى من 12000 جزء في المليون.
كلوريد الفينيل والسرطان
ا كلوريد الفينيل مادة مسرطنة، المرتبط بارتفاع مخاطر الإصابة بسرطان الكبد ، والذي قد يساهم في حدوثه سرطان الدماغ والرئة وكذلك سرطان الجهاز اللمفاوي.
اقرأ أيضا:نترات الأمونيوم - مركب يستخدم في الزراعة ويمكن أن يسبب انفجارات
حدوث كلوريد الفينيل
كلوريد الفينيل يتم إنشاؤه تلقائيًا في البيئة من خلال تحلل بعض المركبات المحتوية على الكلورمن خلال عمل الكائنات الحية الدقيقة. لذلك ، يمكن اعتباره ملوثًا للهواء والماء ، خاصة في المناطق القريبة من مقالب القمامة.
ومع ذلك ، فإن أعلى نسبة حدوث لكلوريد الفينيل تتم عن طريق الطرق الاصطناعية ، المرتبطة بالصناعة الكيميائية ، كما تمت مناقشته سابقًا.
تاريخ كلوريد الفينيل
كان كلوريد الفينيل اكتشف في عام 1835 بواسطة الكيميائي الألماني Justus von Liebig ، عند تفاعل ثنائي كلورو إيثان مع هيدروكسيد البوتاسيوم في بيئة كحولية.
لاحقًا ، في عام 1872 ، لاحظ الكيميائي يوجين باومان ، لأول مرة ، بلمرة كلوريد الفينيل ، الناتج عن PVC ، بعد ترك حاوية تحتوي على مادة معرضة للشمس عن طريق الصدفة.
في عام 1926 ، اكتشف المخترع الأمريكي والدو سيمون إضافات كيميائية توفر مرونة أكبر وقابلية للتكيف لـ PVC ، مما يوسع من إمكانيات تطبيق هذه المادة. حوالي عام 1950 ، بدأ استخدام الـ PVC على نطاق صناعي. حاليًا ، يعد PVC أحد أكثر اللدائن الحرارية استخدامًا في العالم.
بقلم آنا لويزا لورينزن ليما
مدرس كيمياء
هل سمعت من قبل عن عنصر الكلور الكيميائي؟ انقر هنا وتعرف على خصائصها وخصائصها والحصول عليها وتطبيقاتها وتاريخها.
تعرف على التركيب الكيميائي ومصادر الإنتاج وتطبيقات العديد من المركبات العضوية ، مثل الأسيتون والكحول والأثير وغيرها.
تعرف على المزيد حول الخصائص والأنواع والتسميات وأين يمكن العثور على الهيدروكربونات.
تعرف على التركيب الكيميائي لبوليمر PVC (بولي فينيل كلورايد) ، المستخدم على نطاق واسع في إنتاج الأنابيب والمواد الجلدية الاصطناعية.

