عندما نسمع كلمة "سيليكون" نفكر على الفور في زراعة الثدي من خلال الجراحة التجميلية. ومع ذلك ، فإن السيليكون مادة لها عدة أغراض ، بما في ذلك استخدامها في المنتجات التي نستهلكها عادة في حياتنا اليومية.
ولكن قبل النظر إلى هذه التطبيقات ، انظر إلى التركيب الكيميائي للسيليكون وكيف يتم إنتاجه.
ا سيليكون إنها بوليمر التكثيف، أي أن سلاسلها الجزيئية الطويلة تتشكل من خلال تفاعلات بلمرة التكثيف ، حيث تطلق المونومرات ، عندما تتحد ، الماء أو مادة بسيطة أخرى.
ال بنية يتم عرض أساسيات السيليكون أدناه. لاحظ أنه بدلاً من الكربون (C) لدينا السيليكون (Si) كعنصر مركزي ، حيث تتكون السلسلة الرئيسية من السيليكون من ذرات السيليكون بالتناوب مع ذرات الأكسجين. هذا ممكن لأن السيليكون ينتمي إلى نفس العائلة ، في الجدول الدوري ، مثل الكربون ، الذي يأتي في الفترة التي تلي الكربون مباشرة. لذلك ، يحتوي السيليكون على خصائص مشابهة للكربون ، وبالتالي يمكن أن يرتبط بالمجموعات العضوية (R).
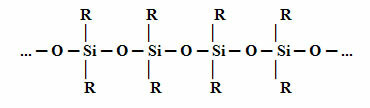
في حالة السيليكون ، فإن المونومرات الأكثر استخدامًا في إنتاجها هي ثنائي كلورو ثنائي ميثيل سيلان أو ثنائي كلورو ثنائي فينيل سيلان. يتم الحصول على هذه المونومرات من خلال التفاعل بين السيليكا ، الموجودة بشكل رئيسي في الرمل ، مع فحم الكوك ، للحصول على السيليكون أولاً:
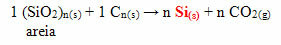
تتمثل الخطوة التالية في تفاعل هذا السيليكون الذي تم الحصول عليه مع كلوريد الميثيل أو مع كلوريد الفينيل لتكوين أحد المونومرين المذكورين أعلاه:
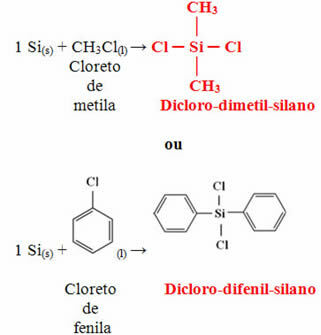
سيتفاعل المونومر الناتج في النهاية مع الماء لتكوين البوليمر (السيليكون) وإطلاق حمض الهيدروكلوريك كمنتج ثانوي:
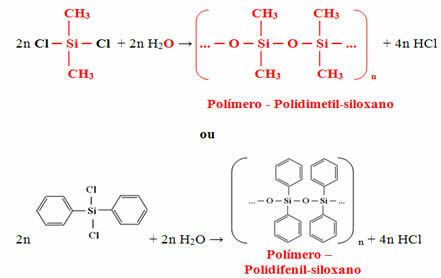
السيليكون عبارة عن بوليمر مستقر للغاية وله مقاومة كبيرة للحرارة ، حيث تبدأ المركبات العضوية المرتبطة بالسيليكون فقط في الاحتراق عند ملامستها للحرارة. ومع ذلك ، عندما تنتهي هذه الجذور من التفاعل ، يبقى السيليكا (الرمل) فقط ، مما يمنع استمرار الاحتراق.
نظرًا لامتلاكها هذه الخصائص ، فهي غير سامة ولها خمول كيميائي كبير وتقدم نفسها بطرق تختلف عن سائل للغاية إلى مادة صلبة شبيهة بالمطاط ، تُستخدم هذه البوليمرات في أكثرها تنوعًا المناطق. فيما يلي بعض هذه التطبيقات:

بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/silicone-constituicao-aplicacoes.htm
