أميدات هي مركبات عضوية نيتروجينية تتميز بوجود مجموعة كربونيل (الكربون الذي يؤدي ارتباطًا مزدوجًا بالأكسجين) ، مرتبطًا مباشرة بالنيتروجين ، والذي بدوره يمكن أن يرتبط بذرتين من هيدروجين.
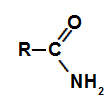
المجموعة الوظيفية من أميد
تصنيف الأميدات
أ) أميد بسيط
و ال الأميد الذي يحتوي على اثنين من الهيدروجين مرتبط بنيتروجين المجموعة الوظيفية.

الصيغة التركيبية لأميد بسيط
ب) أميد أحادي الاستبدال
و ال الأميد الذي يحتوي على هيدروجين واحد فقط مرتبط بنيتروجين المجموعة الوظيفية ، حيث تم استبدال الآخر بجذر عضوي.

الصيغة التركيبية للأميد أحادي الاستبدال
ج) الأميد غير محلول
و ال الأميد التي لا تحتوي على هيدروجين مرتبط بمجموعة النيتروجين الوظيفية ، حيث تم استبدالها جميعًا بجذور عضوية.

الصيغة الهيكلية للأميد غير المستبدل
تسمية الأميدات
قاعدة تسمية IUPAC التي يجب استخدامها لملف الأميد é:
بادئة + إنفكس + أميد
بحيث:
البادئة: تتعلق دائمًا بكمية الكربون الموجودة في السلسلة ؛
Infix: يرتبط دائمًا بنوع الروابط بين ذرات الكربون في السلسلة.
مثال:
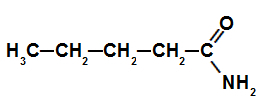
الصيغة التركيبية للأميد مع 5 ذرات كربون
في هذا المثال ، يحتوي الأميد على 5 (بادئة خماسية) ذرات كربون ، وروابط مفردة فقط بين ذرات الكربون. لهذا السبب ، اسمها هو بنتاناميد.
لو أميد متفرعة، سيتم كتابة اسم وموضع كل جذري قبل البادئة ، كما هو متفق عليه. لاحظ المثال أدناه:
مثال: أميد متفرعة
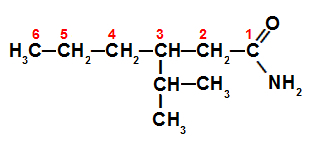
أميد متشعب منظم للتسميات
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
مثل الأميد متفرعة ، من الضروري تحديد سلسلتها الرئيسية (مع أكبر عدد من الكربون من المجموعة الوظيفية) ، والتي تم ترقيمها أعلاه. في هذه الحالة ، تحتوي السلسلة الرئيسية على 6 ذرات كربون (بادئة سداسية عشرية) ، روابط مفردة فقط (إنفكس) بين الكربون وجذر الأيزوبروبيل على الكربون 3. لذلك فإن اسم هذا الأميد هو 3-isopropylhexanamide.
في الأميدات الأحادية المستبدلة أو غير المستبدلة، سيتم دائمًا تحديد موضع الفرع بواسطة N ، نظرًا لأن الجذر مرتبط مباشرة بالنيتروجين. إذا كان هناك شعاعي آخر في السلسلة ، فسيتم كتابته بعد الإشارة إلى الجذر N.
مثال: أميد مستبدل

أميد بديل منظم للتسمية
مثله الأميد، بالإضافة إلى استبدالها ، متفرعة ، فمن الضروري تحديد سلسلتها الرئيسية. وهكذا ، لدينا سلسلة رئيسية بها 6 ذرات كربون (بادئة سداسية عشرية) ، روابط مفردة فقط (إنفكس أ) بين الكربون ، وجذر ميثيل على الكربون 3 وجذر إيثيل على النيتروجين. لذلك ، فإن اسم هذا الأميد هو N-ethyl-3-methylhexanamide.
الخصائص الفيزيائية للأميدات
هم أقل كثافة من الماء.
لديهم طابع أساسي ؛
خاصية الجزيئات القطبية;
القوى الجزيئية التي تربط جزيئات الأميد معًا هي دائم ثنائي القطب;
توجد في حالة صلبة في درجة حرارة الغرفة ، باستثناء الميثاناميد السائل ؛
لديهم قابلية جيدة للذوبان في الماء عندما يكون لديهم عدد قليل من ذرات الكربون. ومع ذلك ، فكلما زاد عدد الكربون ، انخفضت قابلية الذوبان في الماء ، وزادت قابلية الذوبان في المذيبات العضوية ؛
لديهم نقاط انصهار وغليان أعلى بالمقارنة مع المركبات العضوية الأخرى.
استخدامات الأميدات
بشكل عام ، فإن أميدات تستخدم ، على سبيل المثال:
في تركيب (إنتاج) المركبات العضوية المختلفة ؛
في صناعة المتفجرات
في إنتاج اللك (نوع معين من الراتنج) ؛
في إنتاج الأسمدة.
في إنتاج الأدوية ؛
في صناعة الكريمات والمراهم.
بي ديوغو لوبيز دياس
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ بحث:
DAYS ، ديوغو لوبيز. "ما هي الأميدات؟" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-amidas.htm. تم الوصول إليه في 27 يوليو 2021.
كيمياء

الألدهيدات ، مركبات الكربونيل ، مجموعة الكربونيل ، الألدهيدات الرئيسية ، الإيثانال ، المواد الخام في صناعة المبيدات الحشرية والأدوية ، الميتانال ، الفورمالديهايد ، صناعة البلاستيك والراتنج.
الأمينات ، تصنيف الأمينات ، خواص الأمين ، الأمين الأولي ، المركبات العضوية النيتروجينية ، جذور الألكيل ، ثنائي ميثيل أمين ، إيثيل أمين ، ثلاثي ميثيل أمين ، مركبات مستخرجة من الخضروات ، بوتريسين ، كادافيرين ، قواعد عضوية ، توليفات عضوي