البلمرة هو اسم العملية الكيميائية التي ينتج عنها تكوين جزيئات كبيرة (جزيئات كبيرة) تسمى البوليمرات ، من خلال مزيج من الجزيئات الأصغر ، المونومرات.
رد فعل البلمرة إنه شائع جدًا في الطبيعة ، كما نرى في الكربوهيدرات (مثل النشا) والبروتينات (مثل الكازين في الحليب). كما أنه يحدث صناعياً ، لأن الغالبية العظمى من البوليمرات التي يستخدمها البشر في حياتهم اليومية مصنوعة صناعياً.
أول بوليمر ينتج من البلمرة كان مركب الباكليت ، في عام 1909 ، بواسطة الكيميائي البلجيكي ليو هندريك بايكلاند.
بشكل عام ، من أجل دمج مونومر مع آخر (سواء كانا متطابقين أو مختلفين) في تفاعل البلمرة، من الضروري وجود تكافؤ حر (رابطة كيميائية يجب إجراؤها) في كلا المونومرات.
تنشأ هذه التكافؤات نتيجة لانكسار الروابط ، من خلال استخدام المحفزات (مثل النيكل) ، الظروف الخارجية مثل الضوء والحرارة ، أو ظاهرة الرنين في البنية (تحول الإلكترونات).
في تكوين البولي بروبلين (بوليمر PP) ، على سبيل المثال ، المستخدم في الأواني المنزلية ولعب الأطفال ، فإن رابط بي (π) في كل جزيء ينقسم على النحو التالي:
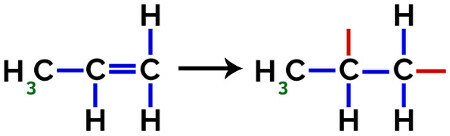
كسر رابطة pi في البروبيلين
وبالتالي ، يمكن لكل مونومر بروبيلين أن يترابط مع اثنين من مونومرات البروبيلين الأخرى ويشكل البوليمر PP أو البولي بروبلين (تشير البادئة بولي إلى عدة وحدات أحادية). الطريقة الأكثر شيوعًا لتمثيل البوليمر تحتوي على المونومر بين الأقواس ، وفي الخارج ، الحرف n ، والذي يشير إلى عدة مونومرات ، كما نرى في حالة بوليمر PP:
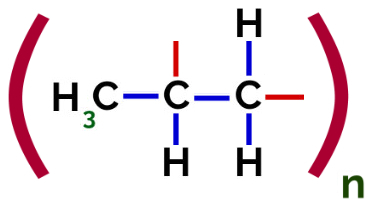
تمثيل بوليمر PP
رد فعل البلمرة بطرق مختلفة كما سنرى أدناه:
أ) رد فعل إضافة البلمرة
في هذا البلمرة، هناك دائمًا انقطاع في رابطة pi في المونومر ، مما يتسبب في ظهور تكافؤين حُر في الهيكل ، كما هو الحال في تكوين بولي ايثيلينوالبوليمر المستخدمة على نطاق واسع في التعبئة والتغليف الصيدلانية.
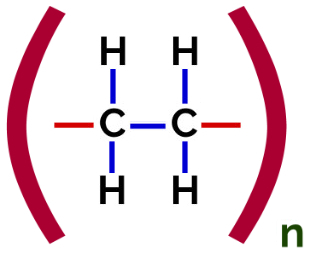
الصيغة الإنشائية للبولي إيثيلين إضافة البوليمر
في البلمرة من البولي إيثيلين ، يتم استخدام جزيئات الإيثيلين (الإيثين) ، التي لها رابطة pi بين ذرتي الكربون ، كمونومر. عندما تنكسر هذه الرابطة ، يظهر تكافؤان حران ، واحد على كل ذرة كربون متضمنة في رابطة pi. تتحد المونومرات بالضبط في كل من هذه التكافؤات ، أي أن تكافؤ أحدهما مرتبط بتكافؤ الآخر ، وهكذا.
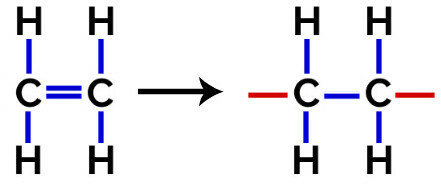
معادلة تشكيل البولي إيثيلين
ب) إضافة تفاعل البلمرة 1.4
في هذه البلمرة ، تقدم المونومرات رابطتين مزدوجتين متناوبتين (واحد باي وسيغما واحد) ، مما يفضل الظاهرة من الرنين (بالتناوب في موضع إلكترونات pi لرابطة pi) ، كما هو الحال في تكوين المطاط الصناعي (polybutadiene)

الصيغة الهيكلية للبولي بوتادين
الوحدة الأحادية لهذا البوليمر هي البوتادين ، التي لها رابطتان مزدوجتان متعاقبتان. مع الرنين ، يكون للهيكل رابطة مزدوجة بين الكربون 2 و 3 ، واثنين من التكافؤات الحرة على الكربون 1 و 4. في هذه التكافؤات الحرة للكربون 1 و 4 بالتحديد تتحد المونومرات.

صدى البوتادين
ج) رد فعل بلمرة التكثيف أو القضاء
إنه رد فعل البلمرة يفقد فيها ، بشكل إلزامي ، مونومرين (متماثل أو مختلف) في نفس الوقت ذرات أو مجموعات ، مما ينتج عنه تكافؤان حُران في كل منهما. بهذه الطريقة ، يتم دائمًا التخلص من الهيدروجين من المونومر ، والذي ينضم بعد ذلك إلى الهالوجين (F ، Cl ، Br ، I) ، OH ، NH2، أو CN للمونومر الآخر.
لذلك ، في البلمرة عن طريق الإزالة ، هناك دائمًا تكوين الماء ، حمض الهالوجين (HCl ، HI ، HF ، HBr) ، الأمونيا (NH3) أو حمض الهيدروسيانيك (HCN) بالإضافة إلى البوليمر. انظر ، على سبيل المثال ، تمثيل تشكيل البوليستر ، مادة تستخدم كنسيج:

معادلة تشكيل البوليستر
المونومرات المكونة للبوليستر هي حمض بنزينديويك و إيثان-1،2-ديول. يمكننا أن نلاحظ ذلك في هذا البلمرة يحدث التخلص من جزيئات الماء ، لأن المونومرين لهما هيدروكسيلان. في هذه العملية ، يفقد الحمض الهيدروكسيلين ، ويفقد كحول الديال الهيدروجين فقط من الهيدروكسيل الخاص به:

هيكل بوليستر
ترتبط مونومرات البوليستر بالأكسجين الموجود في الكحول والكربون الموجود في حمض الكربوكسيل.
بي ديوغو لوبيز دياس
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-polimerizacao.htm