أنت أكاسيد أساسية هم أولئك الذين ، عند التفاعل مع الماء ، يؤدي إلى إنشاء قواعد. عندما تتفاعل مع حمض ، فإنها تشكل الملح والماء.
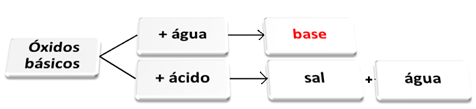
أكاسيد أساسية تتفاعل مع الماء والحمض.
على سبيل المثال ، لدينا أكسيد الصوديوم (Na2O) ، وهو أكسيد قاعدي. انظر أدناه ، عند التفاعل مع الماء ، فإنه يشكل قاعدة هيدروكسيد الصوديوم:
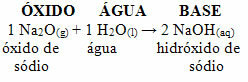
إذا كان نفس هذا الأكسيد يتفاعل مع حمض مثل حمض الكبريتيك (H2فقط4) ، سيتم إنتاج ملح (كبريتات الصوديوم) وماء.
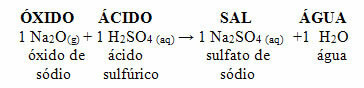
إذا تفاعل أكسيد قاعدي مع أكسيد حمضي ، ينتج الملح أيضًا ، ولكن بدون الماء.
كما هو موضح في المثال الموضح ، فإن الأكاسيد الأساسية الأخرى هي أيضًا مركبات أيونية ، تتشكل فيها في الغالب من المعادن ، العناصر شديدة الحساسية للكهرباء ، وعادة ما تقدم "شحنة" تساوي +1 أو +2.
أمثلة:
في2O = نا1+
ك2يا = ك1+
CaO = Ca2+
MgO = Mg2+
تحتوي هذه المركبات على نقاط انصهار وغليان عالية وجميعها تحيط بأنيون الأكسجين (O2-).
تطبيقات بعض الأكاسيد الأساسية:
• كلب: أكسيد الكالسيوم
يُعرف هذا المركب عمومًا باسم الجير الحي. عند التفاعل مع الماء ، وفقًا للتفاعل أدناه ، يتم تكوين قاعدة (هيدروكسيد الكالسيوم) والتي تستخدم لطلاء الجدران ، جذوع الأشجار وغيرها من المواد ، لغرض رئيسي هو صد الحشرات والحفاظ على الختم ومنع التسلل من الماء. هذه القاعدة المشكلة تسمى
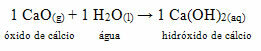

اللوحة البيضاء.
• ك2س: أكسيد البوتاسيوم
يوجد أكسيد البوتاسيوم بشكل شائع في الخشب ورماد السجائر. عند التفاعل مع الماء ، فإنه يشكل هيدروكسيد البوتاسيوم الأساسي (KOH) المستخدم في صناعة الصابون. حتى في الماضي ، في الأماكن التي لا يوجد فيها KOH ، تم استخدام رماد الخضروات ، والذي يحتوي على K2O ، لتتفاعل مع الدهون وتنتج ما يسمى "الصابون الرمادي".
بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/oxidos-basicos.htm
