يمكن أن تخضع الكحوليات للأكسدة عند تعرضها لعامل مؤكسد ، مثل محلول مائي من ثنائي كرومات البوتاسيوم (K2سجل تجاري2ا7) أو برمنجنات البوتاسيوم (KMnO4) في وسط حمضي.
سيهاجم الأكسجين الناشئ [O] في المنتصف الكربون المرتبط بمجموعة الكحول الوظيفية (هيدروكسيل - OH) ، مكونًا مركبًا غير مستقر للغاية ، يسمى ثنائي ديول ، يحتوي على نوعين من الهيدروكسيل مرتبطين بنفس الشيء كربون. نظرًا لأنه غير مستقر ، فإن هذا المركب يطلق الماء ويؤدي إلى منتج جديد.
يعتمد هذا المنتج على نوع الكحول الذي تم تأكسده ، سواء كان أوليًا أو ثانويًا أو ثالثًا أو ميثانول.
باختصار ، لدينا:
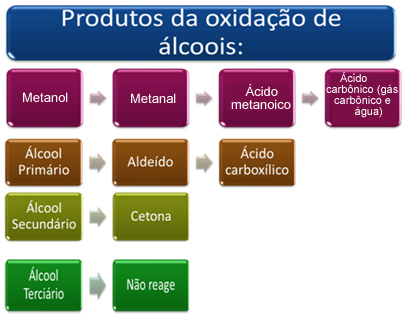
انظر كل حالة أدناه:
- الميثانول (H3C─ أوه):
الميثانول هو الكحول الوحيد الذي يحتوي على ثلاثة هيدروجين مرتبطة بالكربون والتي ستخضع للأكسدة. في هذه الحالة ، نظرًا لوجود ثلاث نقاط على الجزيء يمكن للأكسجين الناشئ مهاجمتها ، ستحدث ثلاث عمليات أكسدة متتالية ، كما هو موضح في الرسم البياني أدناه:
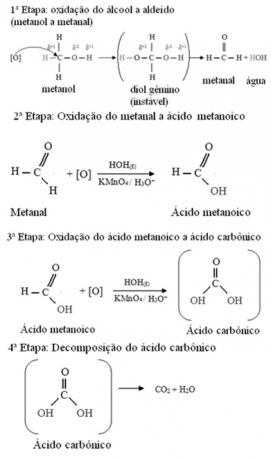
- الكحولات الأولية:
في هذه المركبات ، يرتبط كربون الهيدروكسيل بذرة كربون واحدة فقط ، أي أن الربيطتين الأخريين هما هيدروجين ، وهناك مكانان لهجوم الأكسجين الناشئ.
أولاً ، سيكون هناك تكوين ألدهيد ، كما هو موضح أدناه:
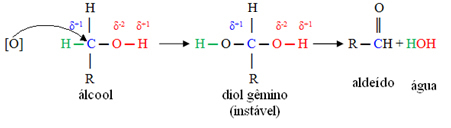
لكن ، تستمر الأكسدة ، لأن الكواشف المستخدمة في أكسدة الكحول أقوى من تلك المستخدمة في أكسدة الألدهيد. ثم يهاجم أكسجين ناشئ آخر الكربونيل وينتج حمض الكربوكسيل.
فيما يلي مثال ، أكسدة الإيثانول ، أولاً إلى الإيثانال ثم إلى حمض الإيثانويك (حمض الأسيتيك). هذا التفاعل الكلي هو تحويل النبيذ إلى خل.
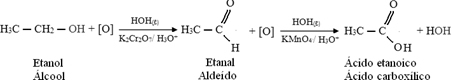
تحدث الأكسدة الجزئية للإيثانول إلى الإيثانيل عندما يأخذ الشخص المدمن على الكحول اختبارًا لمحلل التنفس. يوجد داخل هذا الجهاز خليط صلب من ثنائي كرومات البوتاسيوم والسيليكا في وسط حمضي ، مع حدوث التفاعل التالي:
ك2سجل تجاري2ا7 (aq) + 4 ح2فقط4 (عبد القدير) + 3 CH3CH2أوه(ز) → كر2(فقط4)3 (عبد القدير) +7 صباحا2ا(1) + 3 CH3CHO(ز) + ك2فقط4 (عبد القدير)
البرتقاليالإيثانول (عديم اللون)لون أخضرأثنالي (عديم اللون)
لاحظ أنه بالإضافة إلى أكسدة الإيثانول (الكحول) إلى الإيثانيل (الألدهيد) ، هناك اختزال متزامن لثاني كرومات ، وهو برتقالي ، إلى الكروم (III) ، أو حتى الكروم (II) ، وهو أخضر. سيشير التغيير في اللون إلى أن الشخص يحتوي على نسبة كحول في الدم أكثر من المسموح به.
- الكحولات الثانوية:
هذه مركبات يرتبط فيها كربون الهيدروكسيل بذرتي كربون أخريين وذرة هيدروجين واحدة فقط. لذلك ، سيكون هناك موقع واحد فقط في الجزيء حيث يمكن للأكسجين الناشئ مهاجمته وسيتم تكوين نوع واحد فقط من المنتجات ، والذي سيكون دائمًا عبارة عن كيتون:
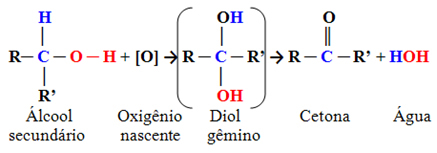
نظرًا لأن الكربون الكربوني للكيتون لا يحتوي على أي هيدروجين مرتبط به مباشرة ، فلم يعد هناك أي احتمال لمزيد من الأكسدة. لذلك ، فإن التفاعل يتوقف عند الكيتون.
- الكحولات الثلاثية:
الكحولات الثلاثية هي تلك التي يصنع فيها الكربون الذي يحتوي على مجموعة -OH ثلاث روابط مع ذرات كربون أخرى. نظرًا لأنها لا ترتبط بالهيدروجين ، فلا فائدة من الجزيء الذي يمكن أن يهاجمه الأكسجين الناشئ. نتيجة لهذه الحقيقة ، لا تخضع الكحولات الثلاثية للأكسدة.
* مصدر ومؤلف الصورة: كوستا.
بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/oxidacao-dos-alcoois.htm


