ا شعاع ذري من العناصر هي خاصية دورية تحدد نصف قطر الذرة والتي تختلف اعتمادًا على موضع العنصر في الجدول الدوري.
وبالتالي ، يمكنهم الزيادة والنقصان مثل العدد الذري (Z) للعنصر الذي يتوافق مع عدد البروتونات الموجودة في نواة الذرات.
باختصار ، نصف القطر الذري يقابل نصف المسافة بين نواة ذرتين متجاورتين ، معبراً عنها على النحو التالي:
ص = د / 2
من أين:
ص = نصف القطر
د = المسافة بين النوى
بشكل عام ، يقاس نصف القطر الذري بوحدات البيكومتر (pm) ، مضاعفات فرعية للمتر (1 بيكومتر = 10-12 م). لاحظ أنه عندما لا يكون المرجع ذرة بل أيونًا ، فإن نصف القطر الموجود هو نصف القطر الأيوني.
تغير نصف القطر الذري
في الجدول الدوري ، يمكن رؤية نمو نصف القطر الذري في الشكل التالي:
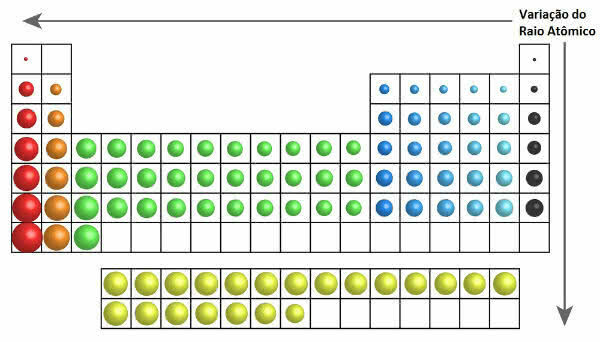 تغير نصف القطر الذري في الجدول الدوري
تغير نصف القطر الذري في الجدول الدوري
وهكذا ، يزداد نصف القطر الذري عموديًا (عائلات أو مجموعات) من أعلى إلى أسفل. على (الفترات) الأفقية ، تزداد من اليمين إلى اليسار.
انظر التباين العكسي في تقارب إلكتروني و كهرسلبية.
طاقة التأين
ال طاقة التأين (أو الكامنة) إنها أيضًا خاصية دورية تحدد الطاقة المطلوبة لتحويل الإلكترون ، والتي يتم التعبير عنها في إلكترون فولت (eV).
اقرأ أيضا: الخصائص الدورية.
تحقق من أسئلة امتحان القبول من خلال التعليق المعلق في: تمارين على الجدول الدوري.