يوضح تحليل الخصائص الفيزيائية والكيميائية للمركبات التي تقوم بالروابط التساهمية (من خلال مشاركة الإلكترونات) أن هناك اختلافات كبيرة بين هذه المواد. لكن قبل أن ننظر إلى هذه الخصائص نفسها ، دعونا نرى الفرق بين المواد الجزيئية والتساهمية.
في المواد الجزيئية هي تلك التي تتشكل عندما ترتبط الذرات من خلال روابط تساهمية ، مما يؤدي إلى ظهور جزيئات ذات عدد محدد.
ومع ذلك ، يمكن أن تنشأ الرابطة التساهمية أيضًا مركبات في بنية شبكة ذات عدد كبير جدًا وغير محدد من الذرات ، وهي الجزيئات الكبيرة. تسمى هذه المواد المركبات التساهمية أو المواد الصلبة للشبكة التساهمية. بعض الأمثلة على هذه المركبات هي: الماس (C) ، الجرافيت (C) ، ثاني أكسيد السيليكون (SiO2) وكربيد السيليكون (SiC).
الآن ، دعونا نلقي نظرة على خصائصه الرئيسية:
- الحالة الفيزيائية في درجة حرارة الغرفة: في ظل الظروف المحيطة ، تم العثور على المركبات الجزيئية والتساهمية في الحالات المادية الثلاث (الصلبة والسائلة والغازية).
أمثلة:
ا صلب: السكر (السكروز) ، السيليكا (الرمل) ، الماس ، الجرافيت ؛
ا سائل: الماء والأسيتون والإيثانول.
ا الغازي: كبريتيد الهيدروجين ، غاز الكلور ، غاز البروم ، غاز الهيدروجين.

- نقطة الانصهار والغليان: بشكل عام ، درجة انصهار وغليان هذه المواد هي أصغر من تلك الموجودة في المواد الأيونية.
المواد التساهمية لها درجات حرارة غليان أعلى من تلك الجزيئية ، ودائما تزيد عن 1000 درجة مئوية. هذا لأنه نظرًا لأن جزيئاتها مرتبطة بشكل وثيق ، وتشكل شبكات بلورية ، فمن الضروري توفير المزيد من الطاقة لجعلها تغير حالتها.
هناك عاملان يتداخلان مع نقاط الغليان والانصهار للمركبات التساهمية والجزيئية: أ الكتلة المولية و ال قوة الجزيئات.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
كلما زادت الكتلة المولية ، زاد القصور الذاتي للجزيء ، وبالتالي ، زادت نقطة الغليان والانصهار. إذا تم تقريب الكتل المولية ، فإننا ننظر إلى القوى بين الجزيئات. أقوى قوة بين الجزيئات هي قوة الرابطة الهيدروجينية ، مما يؤدي إلى درجة غليان وانصهار أعلى. الوسيط هو ثنائي القطب الدائم والأضعف ، مما يؤدي إلى انخفاض نقطة الغليان والانصهار ، هو ثنائي القطب المستحث.
- التيار الكهربائي: في شكلها النقي ، لا تقوم السوائل والمواد الصلبة بتوصيل تيار كهربائي.
الاستثناء هو الجرافيت ، الذي ينقل تيارًا كهربائيًا في صورة صلبة ، لأن إلكترونات الرابطة المزدوجة لها صدى وبالتالي لها قدرة معينة على الحركة.
- الذوبان: يذوب القطبين في القطبين ويذوب غير القطبين في غير قطبي.
- عناد: مقاومة المواد التساهمية للتأثير أو الصدمات الميكانيكية منخفضة. بشكل عام ، هي مواد صلبة هشة ، كما هو موضح في حالة الزجاج ، والذي يتكون من سيليكات الصوديوم والكالسيوم.

- صلابة: بشكل عام ، لديهم صلابة عالية. باستثناء الجرافيت ، لأن ذرات الكربون الخاصة به مرتبطة بثلاث ذرات كربون أخرى ، مكونة ألواح سداسية ذات قابلية معينة للحركة ، مما يجعلها ناعمة. لهذا السبب ، يتم استخدامه حتى كمواد تشحيم.
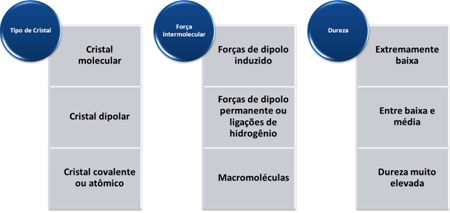
تختلف قساوة هذه المواد حسب نوع البلور كما هو مبين في الجدول أدناه:
بقلم جينيفر فوغاسا
تخرج في الكيمياء
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
فوغا ، جينيفر روشا فارغاس. "خصائص المركبات التساهمية والجزيئية" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm. تم الوصول إليه في 28 يونيو 2021.
المركبات الأيونية ، الخصائص الرئيسية للمركبات الأيونية ، الترابط بين الأيونات ، النقل النهائي للإلكترونات ، قوى الجذب الكهروستاتيكية بين الأيونات ، الأيونات السالبة والموجبة ، الأنيونات ، الكاتيونات ، الترابط الأيوني ، التركيب الجزيئي هو

