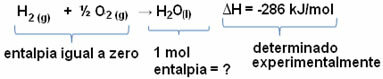
المحفزات هي مواد قادرة على تسريع التفاعل دون تغيير ، أي لا يتم استهلاكها أثناء التفاعل.
لفهم كيفية عمل المحفزات ، نحتاج إلى تذكر ما تم شرحه في النص "طاقة التفعيل”. كما هو موضح هناك ، لكي يبدأ تفاعل كيميائي ، من الضروري أن تمتلك المواد المتفاعلة أو تتلقى قدرًا معينًا من الحد الأدنى من الطاقة ، وهو ما يسمى طاقة التفعيل.
مع هذا الحد الأدنى من الطاقة ، تكون المواد المتفاعلة قادرة على الوصول إلى تنشيط معقدة، وهي حالة وسيطة (حالة انتقالية) تتشكل بين المواد المتفاعلة والمنتجات ، وفيها توجد الروابط السابقة الضعيفة وتشكيل روابط جديدة (موجودة في منتجات).
على سبيل المثال ، ضع في اعتبارك رد الفعل العام أدناه:
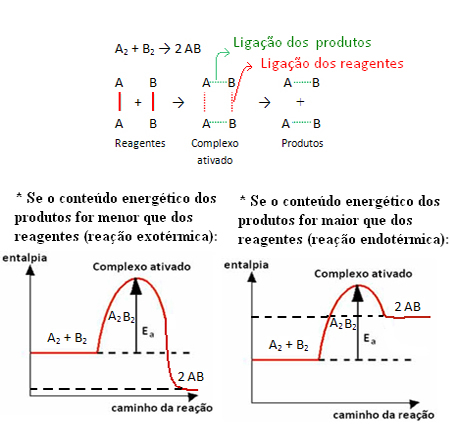
لاحظ أن طاقة التنشيط اللازمة للوصول إلى المركب النشط تصبح نوعًا من العقبة التي يجب التغلب عليها لحدوث التفاعل. هذا يعني أنه كلما زادت طاقة التنشيط للتفاعل ، زادت العقبة التي يجب التغلب عليها وتكون سرعة التفاعل أبطأ.
والعكس صحيح أيضًا ، إذا كانت طاقة التنشيط أقل ، فسيكون التفاعل أسرع. هذا بالضبط ما المحفزات هل هم أنها تخلق مسارًا بديلًا يتطلب طاقة تنشيط أقل ، مما يجعل التفاعل يتقدم بشكل أسرع
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)

من أجل خفض طاقة التنشيط ، يعمل المحفز عن طريق تغيير آلية التفاعل ، عن طريق الدمج مع الكواشف في نظام يمكن أن يكون أحادي الطور (تحفيز متجانس) أو متعدد الأطوار (تحفيز غير متجانس).
يمكن الاطلاع على مزيد من التفاصيل حول هذه الأنواع من الحفز في النصوص أدناه:
- الحفز المتجانس
- تحفيز غير متجانس
لكن ، بشكل عام ، يمكننا القول أن هذا يشكل مزيج المادة المتفاعلة والمحفز مركبًا وسيطًا يتحول بعد ذلك إلى المنتج والمحفز. لاحظ كيف يمكن تمثيل ذلك:
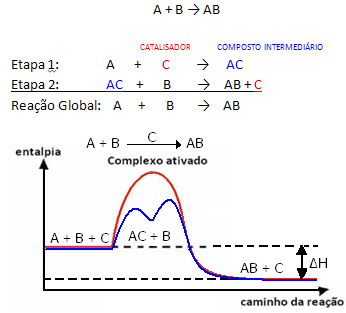
تأكد من أن المحفز يتم تجديده في نهاية التفاعل ، ولا يتم استهلاكه بواسطته.
حقيقة مهمة هي ذلك المحفز يسرع كلا من ردود الفعل الأمامية والعكسية، هذا يعني أنه يقلل من طاقة التنشيط لكليهما.
بقلم جينيفر فوغاسا
تخرج في الكيمياء
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
فوغا ، جينيفر روشا فارغاس. "كيف تعمل المواد الحفازة؟" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/como-atuam-as-substancias-catalisadoras.htm. تم الوصول إليه في 27 يونيو 2021.