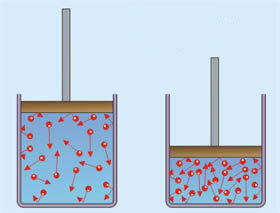
العناصر المسماة المعادن الأرضية القلوية هي تلك التي تنتمي إلى الأسرة 2 أو IIA ، من الجدول الدوري. تتكون هذه المجموعة من العناصر الكيميائية التالية: Be (البريليوم) ، Mg (المغنيسيوم) ، الكالسيوم (الكالسيوم) ، الأب (السترونتيوم) ، Ba (الباريوم) والراديوم (Ra).

لديهم إلكترونان في غلاف التكافؤ ، ويتم تمثيل توزيعهم العام بـ ns2 ، حيث لا يمثل رقم المستوى الأخير. بسبب هذه الخاصية ، فإنها تميل إلى فقدان هذين الإلكترونين ، مما يؤدي إلى 2+ شحنة الكاتيونات.
يشير مصطلح "الأرض" إلى "الموجود على الأرض" ، حيث توجد هذه العناصر ، بشكل أساسي في المعادن. على سبيل المثال ، الكالسيوم في شكل مركب فوسفات الكالسيوم (Ca3(غبار4)2) ، الموجود في قشرة الأرض ويعمل كمادة خام لإنتاج الفوسفور. كما أنه موجود أيضًا في عظام الحيوانات ، لدرجة أنه عندما يتم تحميصها ، يتم الحصول على ما يسمى "وجبة العظام" ، والتي تحتوي على فوسفات الكالسيوم.
من بين معادن الأرض القلوية ، أكثرها تبرزًا هي الكالسيوم انها ال المغنيسيوم.
- الكالسيوم
أيون الكالسيوم (Ca2+) موجود في حوالي 90٪ من عظامنا وأسناننا ؛ وفي الحيوانات يوجد أيضًا في أصدافها. وتتمثل مهمتها في تقوية بنية العظام وتعمل بمثابة مرخي للعضلات. يمكن أن يؤدي نقص الكالسيوم في الجسم إلى تقلصات العضلات والكزاز وهشاشة العظام. لذلك من المهم تناولها من خلال الأطعمة الغنية بالكالسيوم ، مثل الحليب ومشتقاته (الزبدة والجبن وغيرها) واللحوم والخضروات.
من ناحية أخرى ، يمكن أن يسبب الكثير من الكالسيوم ارتخاء العضلات وحصى الكلى وآلام العظام.
بالإضافة إلى الأطعمة المذكورة أعلاه ، لا يزال الكالسيوم موجودًا في أجزاء كثيرة من الطبيعة ، وخاصة في المعادن مثل الكالسيت (CaCO)3) أو كربونات الكالسيوم ، وهو أحد مكونات الحجر الجيري والرخام ، ويستخدم الرخام في صناعة الأحواض والتماثيل والأرضيات والسلالم. كربونات الكالسيوم هي أيضًا منشئ الهوابط والصواعد في الكهوف. يوجد الكالسيوم أيضًا في الجبس الطبيعي (CaSO4. ساعاتين2O) ويسمى الجبس. هذا الملح يمكن أن يجفف ، مما يؤدي إلى CaSO4 اللامائية ، وهي طباشير المدرسة.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
في الصناعة ، يتم إنتاج الجير البكر (CaO) ، الجير المطفأ ، ويسمى أيضًا الجير المطفأ أو الجير المطفأ ، وهو في الواقع هيدروكسيد الكالسيوم (Ca (OH)2) ، وتستخدم في تبييض الدهانات وتحضير الملاط. يسمح التسخين اللطيف للجبس بالحصول على كبريتات الكالسيوم المهدئة ، وهي عبارة عن جبس ، وتستخدم في البناء في إنتاج القوالب في طب الأسنان والطب لحماية كسور العظام ، مثل تلك الموجودة في الذراع الموضح أدناه.
- المغنيسيوم
ايون المغنيسيوم كما أنه ذو أهمية بيولوجية كبيرة ، حيث أنه موجود في 70٪ من عظامنا ، ويفضل عمل الإنزيمات والعضلات والتنسيق الحركي. يمكن أن يؤدي نقصه في الجسم إلى الارتباك وارتفاع ضغط الدم والرعشة وضعف النبض. لذلك يجب أن نتناول الأطعمة التالية التي تحتوي على هذا العنصر: المكسرات والحبوب والخضروات الخضراء. أيضا ، المغنيسيوم الزائد في الجسم يمكن أن يسبب النعاس.
يوجد المغنيسيوم أيضًا في مياه البحر والمعادن. يتم استخدامه في السبائك المعدنية ، مثل المعادن القربانية (التي تتأكسد بدلاً من الفولاذ ، وتمنع تآكله) ، وفي عجلات "المغنيسيوم" وفي الألعاب النارية (تقدم اللونين الفضي والأبيض). مركب مهم جدا من المغنيسيوم هو هيدروكسيد المغنيسيوم (Mg (OH)2) ، والتي ، عند تشتيتها في الماء ، بتركيز 7٪ تقريبًا ، تؤدي إلى معلق معروف شائعًا كحليب المغنيسيا ، الذي يعمل كمضاد للحموضة ، ويحارب حموضة المعدة (حرقة الفؤاد) ملين.

بقلم جينيفر فوغاسا
تخرج في الكيمياء