كما هو موضح في النصوص "الطيف الكهرومغناطيسي للعناصر الكيميائية" و "أطياف الانبعاث والامتصاص وقوانين كيرشوف"، تختلف أطياف الانبعاث المتقطع لكل عنصر كيميائي.

إذن ، لدينا أدناه الأطياف المميزة لبعض هذه العناصر:

وهكذا ، أدرك الفيزيائي الدنماركي نيلز بور (1885-1962) أن هذا يمكن أن يكون مرتبطًا ببنية ذرة كل عنصر من هذه العناصر. لذلك اقترح نموذجًا ذريًا مكملًا لنموذج رذرفورد ، لكنه ركز على سلوك الإلكترونات المحيطة في نواة الذرة.
في وقت سابق ، اقترح ماكس بلانك (1858-1947) نظرية مفادها أن الإلكترونات هي محددة، بمعنى أنهم تنبعث وتمتص كميات محددة من الطاقة ، كما لو كانت حزم صغيرة من الطاقةالذي سماه كم ثمن (الكم، بصيغة المفرد).
لذلك اقترح بور ما يلي: نظرًا لأن كل عنصر له طيف مختلف ، فلكل عنصر في ذراته إلكترونات ذات طاقات ثابتة ومختلفة من عنصر إلى عنصر.
يمكن لكل إلكترون البقاء في مدار معين فقط ، لأنه في كل من هذه المدارات يكون للإلكترون طاقة ثابتة ومحددة جيدًا ومميزة. يمكن للإلكترون أن يشغل فقط مستويات الطاقة التي يمتلك الطاقة الخاصة بها.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
الأطياف متقطعة لأن الإلكترونات مُكممة.
يمكن للإلكترون أن يغير المستويات فقط إذا امتص الطاقة. على سبيل المثال ، عندما تحرق ملح الصوديوم في موقد بنسن ، فإنك تزود الإلكترونات بالطاقة. عند امتصاص كمية من الطاقة ، يقفز الإلكترون إلى مستوى آخر أكثر نشاطًا ، ويبقى في حالة الإثارة. ومع ذلك ، فإن الحالة الأرضية أكثر استقرارًا ، لذلك ينبعث هذا الإلكترون الطاقة الممتصة ويعود إلى مداره الأصلي. تنبعث هذه الطاقة على شكل موجات كهرومغناطيسية يمكن تصورها على شكل ضوء. في حالة الصوديوم ، يكون هذا الضوء أصفر شديد اللون. وهكذا ، عندما تمر هذه الموجات عبر منشور ، يتم الحصول على الطيف المتقطع للصوديوم.
لذلك ، بالنسبة لبور ، يشير كل خط مضيء ظهر في الطيف المتقطع للعناصر إلى الطاقة المنبعثة عندما عاد الإلكترون من مستوى خارجي واحد إلى مستوى أقرب إلى النواة.
يساعد الشكل أدناه على فهم هذه المشكلة بشكل أفضل:
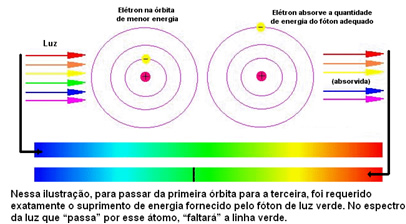
نظرًا لأن ذرات كل عنصر يُسمح لها فقط بقيم طاقة معينة تتوافق مع طبقات الطاقة ، فهناك طيف مختلف لكل عنصر.
بقلم جينيفر فوغاسا
تخرج في الكيمياء
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
فوغا ، جينيفر روشا فارغاس. "الأطياف الكهرومغناطيسية وهيكل الذرة" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/espectros-eletromagneticos-estrutura-atomo.htm. تم الوصول إليه في 27 يونيو 2021.