كان العالم فريدريش كولراوش (1840-1910) أول من اقترح أن المياه النقية توصل الكهرباء ، وإن كان ذلك على نطاق ضيق. هذا لأن الماء يتصرف بطريقة مذبذبة. أي أنه في مناسبات معينة يتصرف مثل الحمض ويتبرع بالبروتونات (H.+); وفي حالات أخرى يتصرف مثل القاعدة ، فيتلقى البروتونات.
هذا يعني أن الماء يقوم بتأين خاص به ، وفقًا للمعادلة الكيميائية الموضحة أدناه:
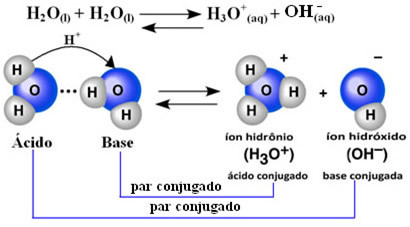
هذه العملية تسمى الأيونات المائية ويحدث على نطاق صغير جدًا ، أي أن الماء عبارة عن إلكتروليت ضعيف جدًا ، مع قيم منخفضة لدرجة التأين وثابت التأين عند التوازن (Kç). هذا هو بالضبط سبب انخفاض الموصلية في الماء.
للحصول على فكرة ، عند درجة حرارة محيطة تبلغ 25 درجة مئوية ، من الممكن تحديد أن تركيزات أيونات الهيدروكسيد والهيدرونيوم المنتجة في التأين الذاتي للماء النقي تساوي 1. 10-7 مول. إل-1. هذا يعني أنه من بين مليار جزيء ماء ، يتأين اثنان فقط.
يسمى ثابت التوازن الأيوني للماء çثابت تفكك الماء ،ثابت التحلل الذاتيأو المنتج الأيوني للماء.هذا الثابت يمثله كث، لأن w تشير إلى الكلمة ماء، والتي تعني في اللغة الإنجليزية الماء.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
يتم حسابها بنفس طريقة حساب ثوابت التوازن الأخرى ، مع تذكر ذلك ، كما هو مذكور في النص "ثوابت Balance Kc و Kp "، في هذه الحالة ، ستظهر المنتجات فقط في التعبير ، لأن الماء في الحالة السائلة له نفس النشاط إلى 1. لا يتم وضع المواد السائلة أو الصلبة النقية في التعبير الثابت للتفكك لأنها لا تتغير. يتم وضع المحاليل المائية والغازية فقط. اذا لدينا:
كث = [ح3ا+]. [أوه-]
كث = (1. 10-7). (1. 10-7)
كث = 10-14
كما هو الحال مع ثوابت التوازن الأخرى ، نعمث يتغير فقط مع تغير درجة الحرارة. مع زيادة درجة حرارة الماء ، يزداد تأينه أيضًا ، مما يعني أن التأين الذاتي للماء هو عملية ماصة للحرارة ، أي أنه يمتص الحرارة.
يمكن ملاحظة ذلك في قيم المنتج الأيوني للماء (K.ث) الوارد في الجدول أدناه عند درجات حرارة مختلفة:
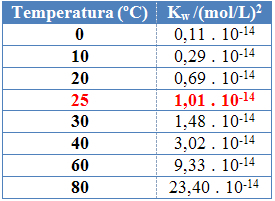
سيكون للمنتج الأيوني للماء دائمًا قيمة ثابتة في كل درجة حرارة ، سواء في الماء النقي أو في المحلول. حتى لو كان المحلول يحتوي على تركيزات من أيونات H3ا+ وأوه- مختلفًا ، سيبقى المنتج بينهما ثابتًا.
بقلم جينيفر فوغاسا
تخرج في الكيمياء
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
فوغا ، جينيفر روشا فارغاس. "منتج الماء الأيوني (Kw)" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/produto-ionico-Agua-kw.htm. تم الوصول إليه في 28 يونيو 2021.


