الذرات عبارة عن جسيمات صغيرة لا متناهية تشكل كل المادة في الكون. بمرور الوقت ، تغيرت فكرة الشكل الذي سيكون عليه التركيب الذري وفقًا لاكتشافات جديدة قام بها العلماء. يمكنك معرفة المزيد عن هذا في النصتطور النموذج الذري.
النموذج هو تمثيل للواقع (وليس الواقع نفسه) ، لذا فإن النماذج الذرية هي تمثيلات لـ المكونات الرئيسية للذرة وهيكلها وتشرح بعض السلوك الفيزيائي والكيميائي للمادة. يتم ذلك لأنه ليس من الممكن بعد للإنسان أن يرى ذرة معزولة حتى باستخدام المجهرات الفائقة.
للحصول على فكرة عن مدى صغر الذرة ، اعرف ذلك ال أصغر جسيم مرئي تحت المجهر العادي يحتوي على أكثر من عشرة مليارات ذرة! الذرة صغيرة جدا، إذا وضعنا مليونًا منهم جنبًا إلى جنب ، فلن نصل إلى سماكة الشعر.
خريطة ذهنية: أتوم
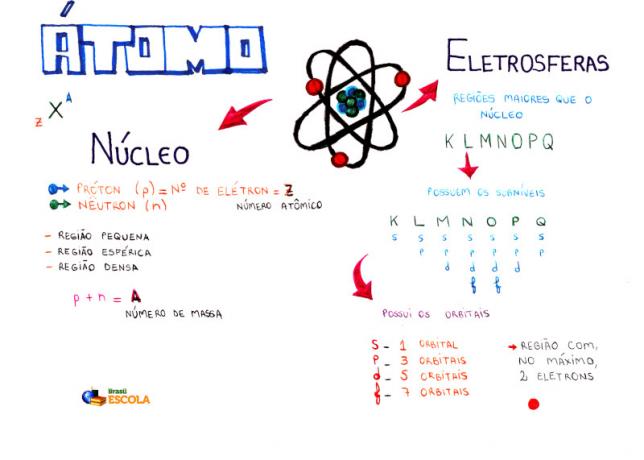
* لتنزيل الخريطة الذهنية بصيغة PDF ، انقر هنا!
من بين النماذج الذرية ، الأكثر استخدامًا حاليًا في المدرسة الثانوية لفهم بنية الذرة وخصائصها هو نموذج Rutherford-Bohr. وفقًا لهذا النموذج ، يتكون هيكل الذرة من جزأين رئيسيين: النواة و ال الغلاف الكهربائي.

جزءان رئيسيان من بنية الذرة - الغلاف الكهربائي والنواة
* النواة: تشكل الجزء المركزي من الذرة ، وهي مدمجة ، ضخمة وكثيفة جدًا ، بالإضافة إلى أنها تتكون من جسيمات ذات كتلة أكبر ، وهي البروتونات والنيوترونات.

شكل توضيحي للبروتونات والنيوترونات التي تشكل النواة الذرية
- البروتونات: إنها جسيمات ذات شحنة كهربائية موجبة (الشحنة النسبية = +1 ؛ الشحن في كولوم (ج) = +1.602. 10-19) وكتلته النسبية تساوي 1.
تم اكتشاف حقيقة أن البروتونات تشكل النواة وتعطيها شحنة موجبة شاملة يوجين غولدشتاين ، في عام 1886 ، من خلال تعديل في أمبولة كروكس وبعض التجارب. ورأى أنه ، في ظل الفولتية العالية جدًا ، ظهرت انبعاثات (أشعة القطب الموجب - بقايا ذرات الغاز التي كانت داخل المصباح والتي انفصلت إلكتروناتها عن طريق التفريغ الكهربائي). عن طريق وضع مجال كهربائي أو مغناطيسي خارج المصباح ، فإن هذه الأشعة تنحرف نحو القطب السالب. هذا يعني أن هناك جسيمات دون ذرية موجبة ، والتي كانت تسمى البروتونات.
لاحقا، إرنست رذرفورد (1871-1937) أجرى التجربة الموصوفة في النص ذرة رذرفوردمما دفعه إلى اكتشاف موقع البروتون: في النواة.
- النيوترونات: إنها جسيمات ذات كتلة مساوية لكتلة البروتونات (1) ، ولكن كما يوحي الاسم ، فهي محايدة ، أي لا تحتوي على شحنة كهربائية.
تم اكتشاف النيوترونات في عام 1932 من قبل جيمس تشادويك (1891-1974) ، الذي أدرك أن نواة البريليوم المشع تنبعث منها جسيمات محايدة كتلتها تساوي تقريبًا كتلة البروتونات (في الواقع ، أكبر قليلاً).
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
يعتمد قطر النواة على كمية البروتونات والنيوترونات الموجودة في الذرة ، ولكنه في المتوسط يبلغ حوالي 10-14 الشهر 10-15 م.
تركز النواة الذرية عمليًا على كتلة الذرة بأكملها ، كونها جزءًا صغيرًا جدًا: كلاً من البروتون والنيوترون أصغر بنحو 100000 مرة من الذرة بأكملها! على سبيل المقارنة ، تخيل أننا نقوم بتوسيع نواة ذرة عنصر الهيدروجين (الذي يحتوي فقط على بروتون) بحجم كرة التنس ، سيكون أقرب إلكترون حوالي ثلاثة كيلومترات من مسافه: بعد! حتى لو تم تكبير الذرة إلى ارتفاع مبنى مكون من 14 طابقًا ، فإن لبها سيكون بحجم حبة ملح في الطابق السابع. إنه حقًا شيء رائع ، ألا تعتقد ذلك ؟!
* المجال الكهربائي: هو المنطقة التي تدور فيها الإلكترونات حول النواة. على الرغم من كونها منطقة ذات حجم أكبر بكثير من النواة ، إلا أنها فارغة عمليًا ، حيث أن كل إلكترون أصغر بمقدار 1836 مرة من بروتون واحد (أو من نيوترون واحد). هذا هو السبب في أن كتلة الذرة عمليا هي كلها في النواة. الإلكترونات هي جسيمات ذات شحنة كهربائية سالبة (-1).
تم اكتشاف الإلكترونات في عام 1897 بواسطة جوزيف جون طومسون (1856-1940) ، خالق نموذج طومسون الذري. يمكن رؤية تجربة طومسون بالتفصيل في النص تجربة طومسون مع التفريغ الكهربائي، ولكن باختصار ، استخدم أمبولة كروكس المذكورة أعلاه وأدرك أن أشعة الكاثود كانت دائمًا ينجذب بواسطة القطب الموجب ، والذي يثبت أن الذرة بها جسيمات سالبة ، والتي تم استدعاؤها الإلكترونات.
تدور الإلكترونات حول النواة بلايين المرات في المليون من الثانية ، وتشكل الذرة وتجعلها تتصرف كما لو كانت صلبة.
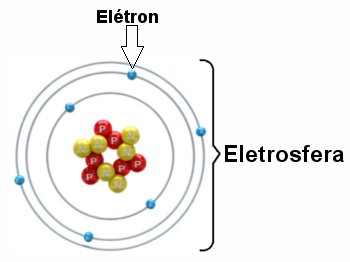
رسم توضيحي للكرة الكهربائية بثلاث طبقات إلكترونية وإلكترونات تدور حول النواة.
باختصار ، يمكننا عمل جدول للتمييز بين الجسيمات دون الذرية الرئيسية الثلاثة التي تشكل جزءًا من بنية الذرة:

الكتلة والشحنة الكهربائية للجسيمات دون الذرية الرئيسية الثلاثة - البروتونات والنيوترونات والإلكترونات
تتكون ذرات جميع العناصر الكيميائية من هذه الجسيمات دون الذرية الثلاثة. ما يميز عنصر كيميائي عن الآخر هو مقدار ظهور هذه الجسيمات ، وخاصة كمية البروتونات في النواة ، وهو ما يسمى بالرقم الذري. استمر في الدراسة حوله من خلال النص. عنصر كيميائي.
* خريطة ذهنية لي ديوغو لوبيز
بقلم جينيفر فوغاسا
تخرج في الكيمياء
كيمياء
تصنيف المادة ، الماء ، غاز الهيدروسيانيك ، ثاني أكسيد الكربون ، الأمونيا ، الهيدروجين ، الهيليوم ، المواد مواد مركبة بسيطة ، مخاليط ، مراحل الخليط ، خليط متجانس ، خليط غير متجانسة.