ا حساب عدد الجسيمات الذرية يستخدم للإشارة إلى كمية البروتونات (في النواة) والإلكترونات (في الغلاف الكهربائي) والنيوترونات (في النواة) الموجودة في أي ذرة أو أيون. للقيام بذلك ، من الضروري معرفة بعض خصائص الذرات:
1- العدد الذري (Z)
إنه رمز رياضي ، يتم تمثيله بالحرف الكبير Z ، موضوع على الجانب الأيسر السفلي من اختصار الذرة:
ضX
يشير إلى عدد البروتونات (p) في النواة وعدد الإلكترونات (e) في الغلاف الكهربائي للذرة. لذلك ، بشكل عام:
Z = p = e
2- العدد الكتلي (أ)
إنه رمز رياضي يتوافق مع مجموع عدد البروتونات (p) والنيوترونات (n) ، وكلاهما موجود في نواة أي ذرة. يتم الحصول على المعادلة التي تمثل العدد الكتلي من خلال:
أ = ص + ن
نظرًا لأن عدد البروتونات يساوي العدد الذري ، فيمكننا كتابة المعادلة لحساب عدد الكتلة على النحو التالي:
أ = ع + ن
إذا عرفنا العدد الكتلي والعدد الذري للذرة ، فيمكننا تحديد عدد النيوترونات على النحو التالي:
ن = أ - ي
3- الأيونات
إنها ذرات تفقد أو تكتسب إلكترونات. لديهم علامة موجبة أو سلبية موضوعة في أعلى يمين تمثيلهم ، كما في النموذج التالي:
X+ أو X-
أيون موجب: يسمى هذا الكاتيون ، وتشير الإشارة الموجبة إلى أنه فقد إلكترونات.
أيون سالب: يسمى هذا أنيون وعلامة سالبة تشير إلى أنه قد اكتسب إلكترونات.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
4- التشابه الذري
أ) النظائر
الذرات التي لها نفس العدد الذري وأعداد كتلة مختلفة. مثال:
7X14 و 7ص16
الذرات X و Y لها نفس العدد الذري (على يسار الاختصار) ، أي يساوي 7. لدى Atom X عدد كتلي (على يمين الاختصار) يساوي 14 ، والذرة Y لها عدد كتلي يساوي 16.
ب) Isobars
الذرات التي لها نفس العدد الكتلي والأعداد الذرية المختلفة. مثال:
15X31 و 13ص31
الذرات X و Y لها رقم كتلي (على يمين الاختصار) يساوي 31. من ناحية أخرى ، تمتلك الذرة X عددًا ذريًا يساوي 15 ، والذرة Y لها عدد ذري يساوي 13.
ج) متساوي التوتر
الذرات التي لها أعداد كتل وأعداد ذرية مختلفة ، ولكن لها نفس عدد النيوترونات.
د) الايزو الكترونيكس
الذرات التي لها نفس عدد الإلكترونات. مثال:
12X+2 و 7ص-3
لدى الذرة X عدد ذري يساوي 12 وهي كاتيون (بشحنة موجبة +2) ، لذلك تفقد إلكترونين ، وبالتالي تحتوي على 10 إلكترونات في غلافها الكهربائي. من ناحية أخرى ، تمتلك الذرة Y عددًا ذريًا يساوي 7 وهي أنيون (بشحنة سالبة -3) ، لذا فهي تكتسب ثلاثة إلكترونات ، وبالتالي تحتوي على 10 إلكترونات في غلافها الكهربائي.
الخريطة الذهنية: الجزيئات الذرية
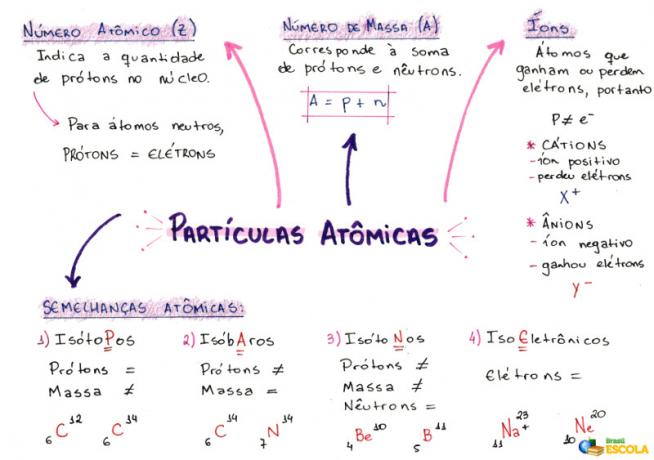
* لتنزيل الخريطة الذهنية بصيغة PDF ، انقر هنا!
أمثلة لحساب عدد الجسيمات الذرية
مثال 1: حدد عدد البروتونات والنيوترونات والإلكترونات في الذرة 14X29.
تم إعطاء القيم التالية للذرة X:
العدد الكتلي (أعلى اليمين) = 29
العدد الذري (أسفل اليسار) = 14
لتحديد عدد البروتونات:
عدد البروتونات يساوي دائمًا العدد الذري ، لذلك تحتوي ذرة X على 14 بروتونًا.
لتحديد عدد الإلكترونات:
نظرًا لأن الذرة X ليست أيونًا ، فإن عدد الإلكترونات يساوي عدد البروتونات ، أي 14.
لتحديد عدد النيوترونات:
يتم تحديد عدد النيوترونات باستخدام عدد الكتلة والبروتونات في الصيغة التالية:
أ = ص + ن
29 = 14 + ن
29-14 = ن
ن = 15
المثال 2: أوجد عدد البروتونات والنيوترونات والإلكترونات للأيون X+3، مع العلم أن العدد الكتلي والعدد الذري هما على التوالي 51 و 23.
تم إعطاء القيم التالية للأيون X:
العدد الكتلي = 51
العدد الذري (أسفل اليسار) = 23
لتحديد عدد البروتونات:
عدد البروتونات يساوي دائمًا العدد الذري ، لذلك تحتوي ذرة X على 23 بروتونًا.
لتحديد عدد الإلكترونات:
الأيون X موجب (+3) ، لذلك فهو كاتيون فقد ثلاثة إلكترونات. لذا فإن عدد إلكتروناتها هو 20.
ملاحظة: يحدث دائمًا انخفاض أو زيادة عدد الإلكترونات بالنسبة إلى العدد الذري.
لتحديد عدد النيوترونات:
يتم تحديد عدد النيوترونات باستخدام عدد الكتلة والبروتونات في الصيغة التالية:
أ = ص + ن
51 = 23 + ن
51 - 23 = ن
ن = 28
المثال 3: تمتلك الذرة W عددًا ذريًا وكتلة مساوية لـ 29 و 57 على التوالي ، أي أنها تساوي a ذرة Y ، التي لها عدد ذري يساوي 30 ، وهو نظير ذرة B ، وعددها الكتلي هو 65. باستخدام هذه المعلومات ، حدد عدد البروتونات والنيوترونات والإلكترونات في الذرة ب.
البيانات التي يوفرها التمرين:
أتوم دبليو
العدد الذري (أسفل اليسار) = 29
العدد الكتلي (أعلى اليمين) = 57
Y isobar ، أي أن كتلة Y تساوي أيضًا 57.
ذرة
العدد الذري = 30
العدد الكتلي = 57
بهاتين القيمتين ، يجب أن نحدد رقمه النيوتروني لأنه متساوي للعنصر B:
أ = ع + ن
57 = 30 + ن
57 - 30 = ن
ن = 27
قبر:
العدد الكتلي = 65
عدد النيوترونات = 27
بهذه البيانات يجب أن نحدد عددها الذري ، لأننا بذلك نحدد عدد البروتونات وعدد الإلكترونات (بما أنه ليس أيونًا):
أ = ع + ن
65 = Z +27
65 - 27 = ض
ض = 38
لذلك ، تحتوي الذرة B على 38 بروتونًا و 38 إلكترونًا و 27 نيوترونًا.
* خريطة ذهنية بقلم فيكتور ريكاردو فيريرا
مدرس كيمياء
بي ديوغو لوبيز دياس