في ال ردود فعل الإضافةفي الألكينات(الهيدروكربونات التي لها رابطة مزدوجة بين ذرتين من الكربون) ، يتم كسر رابطة pi بين ذرتين من الكربون ويلتصق كل من الكربون بذرة جديدة. نظرة:
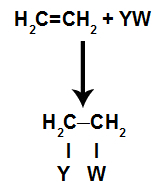
نموذج تخطيطي عام لرد فعل إضافة
مبادئ تفاعل الإضافة
أ) كسر وصلة باي
يتم كسر رابطة pi بسهولة لأنها رابطة أضعف من رابطة سيجما. ومع ذلك ، لكي يحدث هذا ، من الضروري أن يخضع الألكين لظروف توفر هذا الاضطراب. بعد كسر رابطة pi بين ذرتين من الكربون ، يظهر موقع الترابط (للذرات الجديدة) دائمًا على كل من ذرات الكربون المعنية.
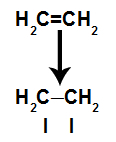
رسم تخطيطي يصور كسر وصلة باي
ب) شروط كسر رابطة باي
العوامل التي تفضل كسر رابطة pi هي:
استخدام المحفزات
تدفئة؛
وجود حمض في وسط التفاعل.
ج) حدوث تفاعل الإضافة
سيتم دائمًا احتلال مواقع الربط التي تم إنشاؤها بعد كسر الرابطة pi بواسطة ذرات المادة المتفاعلة الموجودة في نفس الحاوية مثل الألكين. تمت تسمية تفاعل الإضافة على اسم نوع الكاشف الممزوج بالألكين.
أنواع تفاعلات الإضافة في الألكينات
أ) الهدرجة
يتم خلط ألكين بغاز الهيدروجين (H.264)2) في وعاء وتعرض لعمل محفز صلب (نيكل أو بلاتين أو بلاديوم) وتسخين (Δ).
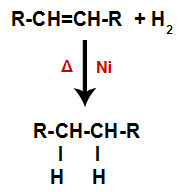
مخطط عام لتفاعل الهدرجة في الألكينات
يتسبب وجود المحفز والتسخين في وجود رابطة pi للألكين ورابطة سيجما بين هيدروجين H2 يتم كسرها بسرعة أكبر. مع ذلك ، يكون لدينا إنشاء موقعين للترابط في الألكين وذرتي هيدروجين حرتين في وسط التفاعل.

إنشاء مواقع ربط وفصل الذرة
وهكذا ، بعد ذلك مباشرة ، تحتل كل ذرة هيدروجين حرة أحد مواقع الترابط المتكونة في الألكين. نظرًا لأن المادة المتكونة تحتوي فقط على الكربون والهيدروجين ، بالإضافة إلى الروابط البسيطة فقط بين الكربون ، فهي عبارة عن ألكان.
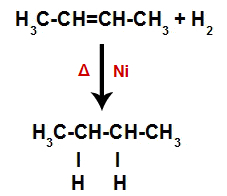
معادلة تمثل تكوين الألكان في الهدرجة
ب) الهلجنة
يتم خلط ألكين بمواد بسيطة (F2، Cl2، ر2 مهلا2) التي شكلتها الهالوجينات (الكلور والفلور واليود والبروم) في وعاء وتعرض لتأثير الضوء (λ) والتدفئة (Δ).

مخطط عام لتفاعل الهالوجين في الألكينات
يعمل تأثير الضوء والتدفئة على جعل رابطة pi للألكين ورابطة سيجما بين المواد المكونة من الهالوجين لتتكسر بسرعة أكبر. وبهذا ، يكون لدينا إنشاء موقعين للربط في الألكين وذرتي هالوجين حرتين في وسط التفاعل.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)

إنشاء مواقع ربط وفصل الذرة
وبالتالي ، بعد ذلك مباشرة ، تحتل كل ذرة هالوجين حرة أحد مواقع الترابط المتكونة في الألكين. نظرًا لأن المادة المتكونة تحتوي على هالوجين مرتبط بهيكل مكون من الكربون والهيدروجين ، فهو عبارة عن أ هاليد عضوي.

معادلة تمثل تكوين هاليد عضوي في الهالوجين
ج) الترطيب
يتم خلط ألكين بالماء (H2س) في حاوية وتعرض لعمل محفز (في هذه الحالة ، حمض الكبريتيك).
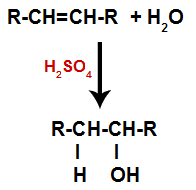
المخطط العام لتفاعل الماء في الألكينات
يؤدي وجود حامض الكبريتيك في التفاعل إلى تكسر رابطة pi للألكين ورابطة سيجما بين الهيدروجين (H) والهيدروكسيل (OH) بسرعة أكبر. وبذلك ، يكون لدينا إنشاء موقعين للربط في الألكين وواحد هيدروجين حر وآخر هيدروكسيل في وسط التفاعل.
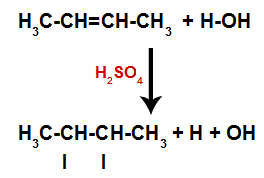
إنشاء مواقع ربط وفصل الذرة
وهكذا ، بعد ذلك بوقت قصير ، يحتل الهيدروجين والهيدروكسيل أحد مواقع الترابط المتكونة في الألكين. نظرًا لأن المادة المتكونة تحتوي على هيدروكسيل مرتبط بكربون مشبع (فإنه يصنع روابط بسيطة فقط) ، فهو كحول.
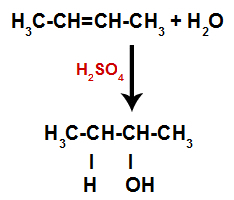
معادلة تمثل تكوين الكحول في الماء
د) الإضافة بهاليدات الهيدروجين
يتم خلط ألكين مع حمض غير عضوي مهلجن (HF ، HI ، HCl ، HBr) في وعاء.

مخطط عام لتفاعل حمض هاليد في الألكينات
يؤدي وجود الحمض في التفاعل إلى تكسر رابطة pi للألكين بسرعة أكبر. تتكسر الرابطة المفردة في الحمض لأن هذه المواد تتأين بشكل طبيعي. وبالتالي ، يتم إنشاء موقعي ربط في الألكين وهناك وجود هيدروجين وهالوجين حر في وسط التفاعل.
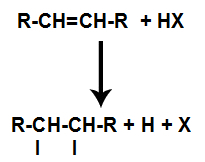
إنشاء مواقع ربط وفصل الذرة
وهكذا ، بعد ذلك بوقت قصير ، احتل الهيدروجين والهالوجين أحد مواقع الترابط المتكونة في الألكين. نظرًا لأن المادة المتكونة تحتوي على هالوجين مرتبط بهيكل مكون من الكربون والهيدروجين ، فهو هاليد عضوي.
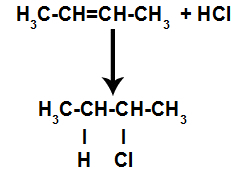
معادلة تمثل تكوين هاليد عضوي في الهالوجين
بي ديوغو لوبيز دياس
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
DAYS ، ديوغو لوبيز. "تفاعلات الإضافة في الألكينات" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/reacoes-adicao-alcenos.htm. تم الوصول إليه في 28 يونيو 2021.
كيمياء

الألكانات ، الهيدروكربونات ، الميثان ، السلسلة المشبعة ، الأليفاتية ، البارافينات ، الوقود ، البنزين ، الشمع المعدني ، البترول ، الصخر الزيتي ، الغاز الطبيعي ، صناعة البتروكيماويات.
كيمياء

الألكينات ، الغاز ، الإيثيلين ، الإيثيلين ، البلاستيك ، المطاط الصناعي ، الأصباغ ، الأقمشة الاصطناعية ، المتفجرات ، تكسير البترول ، البولي إيثيلين ، الغاز الأوليفينات ، الهيدروكربونات ، السلسلة ثاني أكسيد الكربون غير الحلقي.
الألكاينات ، الهيدروكربونات الأخلاقية ، الهيدروكربونات الأسيتيلية ، سلسلة الكربون غير الحلقية ، سلسلة الكربون متجانسة ، سلسلة كربون غير مشبعة ، رابطة ثلاثية ، بولي كلوريد الفينيل ، PVA ، الأسيتيلين ، المطاط الصناعي ، البلاستيك ، الأسلاك المنسوجات.