На температуру кипения органических соединений влияют два фактора: тип межмолекулярного взаимодействия и размер молекулы.
Чем больше размер молекулы, тем выше температура ее кипения.
Наблюдайте за структурами и их соответствующими T.E .: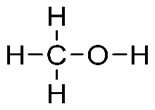 ТЫ. (° С): 64,5
ТЫ. (° С): 64,5
Метанол
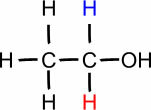 ТЫ. (° С): 78,3
ТЫ. (° С): 78,3
Спирт этиловый
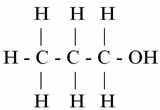 ТЫ. (° С): 97,2
ТЫ. (° С): 97,2
Пропанол
Обратите внимание, что по мере увеличения количества атомов углерода в молекуле температура кипения становится выше. Таким образом, метанол, который имеет только один атом углерода, кипит при 64,5 ° C, а пропанол (3 атома углерода) достигает только своей T.E. при 97,2 ° С.
Но в молекулах одинакового размера? Как узнать, у кого T.E. выше?
Определит тип межмолекулярного взаимодействия.
Пример: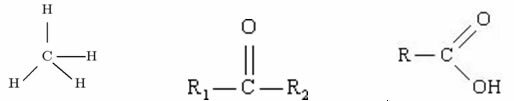
Метанкетонкарбоновая кислота
У какой из этих трех органических структур самый высокий Т.Э.?
В этом случае мы не можем полагаться на размер молекулы, как делали раньше, поскольку три структуры в этом отношении не различаются.
Сейчас применяется правило: чем выше интенсивность межмолекулярных сил, тем выше температура кипения.
Индуцированный диполь
По возрастанию интенсивности →
Основываясь на этой шкале интенсивности, посмотрите, какие силы преобладают в молекулах:
Метан: диполь-индуцированный
Кетон: диполь-диполь
Карбоновая кислота: водородные связи
С помощью этого мы можем классифицировать, какая из этих молекул имеет самую высокую температуру кипения: Кислота карбоновая кислота имеет более высокую ТЭ. потому что водородная связь, присутствующая в этом соединении, имеет наибольшую интенсивность.
Метан
По возрастанию интенсивности →
Эта схема показывает, что у метана самая низкая точка кипения из-за преобладающего типа межмолекулярной силы (индуцированный диполь).
Лирия Алвес
Окончила химический факультет
Бразильская школьная команда
Узнать больше!
Полярность органических соединений
Органическая химия - Химия - Бразильская школа
Источник: Бразильская школа - https://brasilescola.uol.com.br/quimica/temperatura-ebulicao-dos-compostos-organicos.htm