THE distilație fracțională este un procedeu folosit pentru separarea amestecurilor omogene formate din cel putin doua lichide miscibile. Separarea prin această metodă se bazează pe diferitele puncte de fierbere ale componentelor amestecului.
Acest tip de separare se aplică în general amestecurilor care au componente cu o diferență de punct de fierbere de aproximativ 25 °C.
Aparatul principal pentru proces este coloană de fracţionare, numită și coloană de distilare, care are în interior o serie de obstacole pentru a împiedica volatilizarea tuturor componentelor amestecului în același timp.
Practic, amestecul este încălzit într-un balon de distilare până când starea fizică a componentei cu punctul de fierbere cel mai scăzut se modifică. Apoi, aburul trece printr-o coloană fracționată, care separă fracțiile, iar după aceea, condensatorul face ca substanța să revină la starea lichidă, astfel încât să fie direcționată către recipientul de colectare.
Distilarea fracționată este utilizată pe scară largă în industrii și laboratoare, având o mare semnificație comercială. Exemple de aplicații sunt: purificarea apei, separarea componentelor petroliere și separarea aerului lichefiat.
Petrolul, de exemplu, este un amestec de hidrocarburi, cum ar fi butan (PE 20 °C), benzină (PE 150 °C) și kerosen (PE 300 °C). Prin urmare, ordinea de separare a componentelor în distilare fracționată de la punctul de fierbere cel mai scăzut la cel mai ridicat este: butan, benzină și kerosen.
Echipament de distilare fracționată
La distilarea fracționată, se utilizează un sistem compus din următoarele părți:
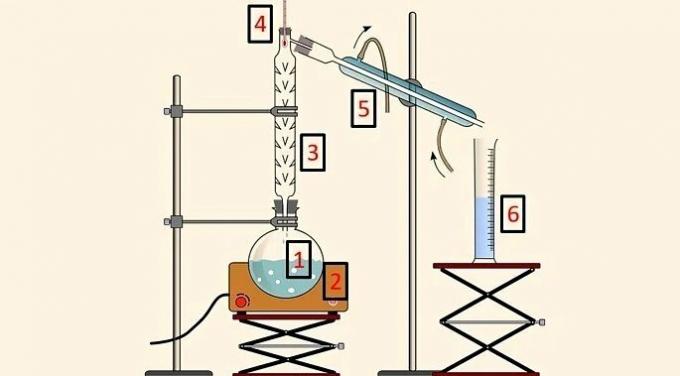
- Balon de distilare (1), care conține amestecul;
- Pătură de încălzire (2), care asigură căldură amestecului;
- Coloana de distilare (3), care permite separarea in functie de temperatura;
- Termometru (4), pentru a urmări schimbarea temperaturii;
- Condensator (5), pentru a răci componenta evaporată;
- Pahar (6), pentru a colecta componenta separată în stare lichidă.
Proces de separare în distilare fracționată
Mai întâi, amestecul este plasat în balonul de distilare împreună cu granulele anti-coliziune pentru a preveni evaporarea rapidă.
Coloana fracţionată este conectată la balonul de distilare. Pe măsură ce amestecul este încălzit, aburul se ridică în coloană, al cărei interior este căptușit cu „obstacole”, de obicei din margele de sticlă sau porțelan.
Contactul fluidului din interiorul coloanei face ca substanțele din amestec să piardă căldură la trecerea prin echipament și doar componenta cu punctul de fierbere cel mai scăzut merge în vârful coloanei.
Vaporii care ajung la condensator sunt apoi raciti pana se lichefiaza, adica revin in stare lichida si sunt colectati in balonul receptor.
Citeste si: Ce este distilarea?
Distilarea fracționată a petrolului
Uleiul este un amestec complex de compuși organici și diferitele componente separate în procesul de distilare se numesc fracții. Fracțiile de petrol sunt formate din hidrocarburi, precum benzină, motorină, kerosen și bitum.
Fracțiile sunt separate în turn de distilare, o coloană de oțel umplută cu tăvi care au „obstacole” pentru trecerea uleiului.
Inițial, uleiul este încălzit într-un cuptor și amestecul încălzit este alimentat la fundul unui turn de distilare. Temperatura turnului este mai mare în partea de jos și mai mică în partea de sus pentru a preveni evaporarea fracțiilor mai grele cu componentele mai ușoare.
Hidrocarburile cu lanț de carbon mai lung sunt condensate și îndepărtate în partea de jos a turnului. Aceste fracții sunt întunecate, vâscoase și mai greu de evaporat. Cele cu un singur lanț, în schimb, au puncte de fierbere mai mici și, prin urmare, se condensează la temperaturi mai apropiate de vârful turnului, unde sunt colectate.
afla mai multe despre rafinarea petrolului.
Diferența dintre distilare simplă și fracționată
Distilarea simplă se aplică atunci când dorim să separăm un solid dizolvat într-un lichid. Pentru aceasta, încălzim amestecul până când solventul se evaporă. Acest proces este mai rapid și necesită mai puțină energie decât distilarea fracționată.
Un exemplu de amestec care poate fi separat prin distilare simplă este apa și sarea. Apa, având un punct de fierbere mult mai mic decât sarea de masă, se evaporă la încălzirea amestecului și, după trecerea printr-un condensator, se colectează într-un alt recipient.
Distilarea fracționată se aplică la separarea lichidelor care sunt miscibile între ele, cum ar fi apa și acetona.
Obține mai multe cunoștințe cu conținutul:
- Distilare simplă și fracționată
- Separarea amestecului
- Exerciții de separare a amestecurilor
Referințe bibliografice
MARO, T. L.; LEMAY JR., H. ȘI.; BURSTEN, B. ȘI.; BURDGE, J. R. Chimia știința de bază. a 9-a ed. Pearson Prentice Hall din Brazilia, 2008.
USBERCO, J.; SALVADOR, E. Chimie generală. a 12-a ed. Sao Paulo: Saraiva, 2006.
RUSSELL J B. Chimie generală. vol. 1. Makron, 1996.
- Distilare
- Distilare simplă și fracționată
- rafinarea petrolului
- Exerciții de separare a amestecurilor
- Separarea amestecurilor
- Materiale utilizate în laboratorul de chimie
- sticla de laborator
- Exerciții de chimie organică cu răspunsuri
