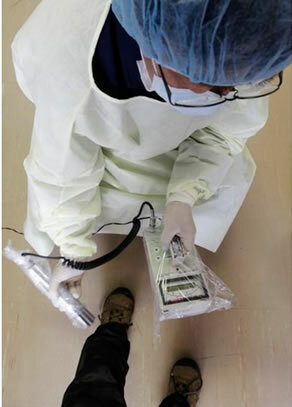
Niobiul (Nb) este elementul chimic al numărului atomic 41 aparținând grupei 5 din tabelul periodic.
Este un metal de tranziție disponibil în mod natural în stare solidă, care a fost descoperit în 1801 de chimistul britanic Charles Hatchett.
Mineralele care conțin niobiu sunt rare în lume, dar abundente în Brazilia, țara cu cele mai mari rezerve de acest metal.
Datorită proprietăților sale, conductivității ridicate și rezistenței la coroziune, acest element are multe aplicații, de la producția de oțel până la fabricarea rachetelor.
Apoi, vom introduce acest element chimic și caracteristicile care îl fac atât de important.
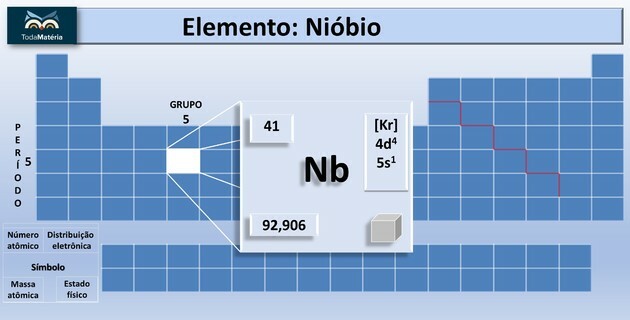
Ce este niobiul?
Niobiul este un metal refractar, adică este foarte rezistent la căldură și uzură.
Metalele din această clasă sunt: niobiu, tungsten, molibden, tantal și reniu, niobiul fiind cel mai ușor dintre toate.
Niobiul apare în natură în minerale, de obicei legate de alte elemente, în principal tantal, deoarece cele două au proprietăți fizico-chimice foarte similare.
Acest element chimic este clasificat ca un metal de tranziție pe tabelul periodic. Este luminos, cu duritate redusă, cu rezistență scăzută la trecerea curentului electric și rezistent la coroziune.
Proprietățile fizice ale niobiului
| starea fizică | solid la temperatura camerei |
|---|---|
| culoare și aspect | gri metalizat |
| Densitate | 8,570 g / cm3 |
| Punct de fuziune | 2468 ° C |
| Punct de fierbere | 4742 ° C |
| Structură cristalină | Cubic centrat pe corp - CCC |
conductivitate termică |
54,2 W m-1 K-1 |
Proprietățile chimice ale niobiului
| Clasificare | metal de tranziție |
|---|---|
| numar atomic | 41 |
| bloc | d |
| grup | 5 |
| Curs de timp | 5 |
| greutate atomica | 92.90638 u |
| raza atomica | 1,429 Å |
| ioni comuni | Nb5+ și Nb3+ |
| electronegativitate | 1.6 Pauling |
Principalul avantaj al utilizării acestui metal este că doar o cantitate, în grame, din acest element poate modificați o tonă de fier, făcând metalul mai ușor, rezistent la coroziune și multe altele eficient.
Unde se găsește Niobiu?
În comparație cu alte substanțe prezente în natură, niobiul are o concentrație scăzută, în proporție de 24 de părți pe milion.
Acest metal se găsește în următoarele țări: Brazilia, Canada, Australia, Egipt, Republica Democrată Congo, Groenlanda, Rusia, Finlanda, Gabon și Tanzania.
Niobiu în Brazilia
În anii 1950, cel mai mare zăcământ de minereu de piroclor, care conține acest metal, a fost descoperit în Brazilia de geologul brazilian Djalma Guimarães.
Cantitatea mare de minereuri care conțin niobiu se află în Brazilia, cel mai mare producător din lume, care deține mai mult de 90% din rezervele metalice.
Rezervațiile explorate sunt situate în statele Minas Gerais, Amazonas, Goiás și Rondônia.
minereuri de niobiu
Niobiul se găsește în natură întotdeauna legat de alte elemente chimice. Peste 90 de specii minerale care conțin niobiu și tantal în natură sunt deja cunoscute.
În tabelul de mai jos, putem vedea câteva din minereurile care conțin niobiu, principalele caracteristici și conținutul de niobiu disponibil în fiecare material.
| tantalit columbit | |
|---|---|
 | |
| Compoziţie: | (Fe, Mn) (Nb, Ta)2O6 |
| Conținut de niobiu (maxim): | 76% din Nb2O5 |
| Caracteristici: |
|
| Piroclorit | |
|---|---|
 | |
| Compoziţie: | (La2,Aici)2(Nb, Ti) (O, F)7 |
| Conținut de niobiu (maxim): | 71% din Nb2O5 |
| Caracteristici: |
|
| Loparite | |
|---|---|
 | |
| Compoziţie: | (C, Na, C)2(Ti, Nb)2O6 |
| Conținut de niobiu (maxim): | 20% din Nb2O5 |
| Caracteristici: |
|
explorarea niobiului
Minereurile de niobiu suferă transformări până la formarea produselor care vor fi comercializate.
Etapele procesului pot fi rezumate ca:
- Minerit
- Concentrația de niobiu
- Rafinare cu niobiu
- Produse cu niobiu
Exploatarea minieră are loc acolo unde există rezerve de minereu, care sunt extrase folosind explozivi și transportate cu centuri la locul unde are loc etapa de concentrare.
Concentrarea are loc odată cu descompunerea minereului, măcinarea face ca cristalele de minereu să devină mult mai fine și folosind separare magnetică fracțiunile de fier sunt îndepărtate din minereu.
În rafinarea cu niobiu, sulful, apa, fosforul și plumbul sunt îndepărtate.
Unul dintre produsele care conțin niobiu este aliajul fier-niobiu, care este produs în conformitate cu următoarea ecuație:
Acest proces se numește aluminotermie în care concentratul de minereu este amestecat în reactoare cu resturi de fier sau oxid de fier.
Oxizii metalici reacționează cu aluminiul la temperaturi ridicate, generând produsul de interes.
Cele mai comercializate produse de niobiu sunt:
- Concentrate de niobiu: o bază care conține 58% Nb2O5.
- Aliaj fier-niobiu: conține 65% niobiu.
- Oxid de înaltă puritate: utilizat la producerea de materiale speciale.
Pentru ce este niobiul?
Caracteristicile niobiului fac ca acest element să fie din ce în ce mai de dorit și cu nenumărate aplicații.
De la descoperirea sa în 1905, aplicațiile pentru niobiu au început să fie cercetate, când chimistul german Werner von Bolton a produs elementul în formă pură.
Anii 50 au reprezentat o căutare excelentă pentru aplicații de niobiu, deoarece până atunci nu a fost produsă pe scară largă.
În această perioadă, războiul rece a stârnit interesul ca acest metal să fie utilizat în componentele aerospațiale.
Mai jos este o listă a modurilor în care este utilizat niobiul.
Aliaje metalice

Adăugarea de niobiu la un aliaj mărește întărirea acestuia, adică capacitatea de întărire atunci când este expusă la căldură și apoi răcită. Astfel, materialul care conține niobiu poate fi supus unor tratamente termice specifice.
Afinitatea niobiului cu carbonul și azotul favorizează proprietățile mecanice ale aliajului, crescând, de exemplu, rezistența mecanică și rezistența la uzura abrazivă.
Aceste efecte sunt benefice deoarece pot extinde aplicațiile industriale ale unui aliaj.
Oțelul, de exemplu, este un aliaj metalic format din fier și carbon. Adăugarea de niobiu la acest aliaj poate avea avantaje pentru:
- Industria auto: producerea unei mașini mai ușoare și mai rezistente la coliziune.
- Constructie: îmbunătățește sudabilitatea oțelului și oferă maleabilitate.
- Industria conductelor de transport: Permite construcții cu pereți mai subțiri și diametre mai mari, fără a afecta siguranța.
super aliaje

Superaliajul este un aliaj metalic cu rezistență ridicată la temperaturi ridicate și rezistență mecanică. Aliajele care conțin niobiu fac ca acest material să fie util în fabricarea turbinelor aeronavei sau în producția de energie.
Avantajul funcționării la temperaturi ridicate face ca super-aliajele să compună motoare cu reacție de înaltă performanță.
magneți supraconductori

Superconductivitatea niobiului determină utilizarea compușilor niobiu-germaniu, niobiu-scandiu și niobiu-titan în:
- Scanner de aparate RMN.
- Acceleratoare de particule precum Large Hadron Collider.
- Detectarea radiației electromagnetice și studiul radiației cosmice de către materiale care conțin nitrit de niobiu.
Oxizi
Alte aplicații pentru niobiu sunt sub formă de oxizi, în principal Nb2O5. Principalele utilizări sunt:
- lentile optice
- Condensatoare ceramice
- senzori de pH
- părțile motorului
- Bijuterii
Istoria și descoperirea niobiului
În 1734, unele minereuri aparținând unei colecții personale a lui John Winthrop au fost transportate din America în Anglia, iar aceste obiecte au făcut parte din colecția British Museum din Londra.
La aderarea la Societatea Regală, chimistul britanic Charles Hatchett s-a concentrat pe investigarea compoziției minereurilor disponibile la muzeu. Acesta este modul în care, în 1801, a izolat un element chimic, sub formă de oxid, și l-a numit columbiu și minereul din care a fost extras columbit.
În 1802, chimistul suedez Anders Gustaf Ekeberg a raportat descoperirea unui nou element chimic și l-a numit tantal, cu referire la fiul lui Zeus din mitologia greacă.
În 1809, chimistul și fizicianul englez William Hyde Wollaston a analizat aceste două elemente și a observat că acestea au caracteristici foarte asemănătoare.
Datorită acestui fapt, din 1809 până în 1846, columbiul și tantalul au fost considerate același element.
Mai târziu, mineralogul și chimistul german Heinrich Rose, investigând minereul de columbit, a observat că tantalul era și el prezent.
Rose a găsit prezența unui alt element, asemănător tantalului și l-a numit Niobius, cu referire la Niobe, fiica lui Tantalus, din mitologia greacă.
În 1864, suedezul Christian Bromstrand a reușit să izoleze niobiul dintr-o probă de clorură încălzită într-o atmosferă de hidrogen.
În 1950, Uniunea Chimiei Pure și Aplicate (IUPAC) a aprobat niobiul ca denumire oficială, mai degrabă decât columbiu, deoarece erau același element chimic.
Rezumatul niobiului
Element chimic: Niobiu | |||
|---|---|---|---|
| Simbol | Nb | Descoperitor | Charles Hatchett |
| numar atomic | 41 | masă atomică | 92.906 u |
| grup | 5 | Curs de timp | 5 |
| Clasificare | metal de tranziție | Distribuție electronică | [Kr] 4d35s2 |
| Caracteristici |
|
||
| Minereuri principale |
|
||
| Principalele produse |
|
||
| aplicații |
|
||
| Apariție | In lume |
|
|
| In Brazilia |
|
Exerciții inemice și examene de admitere
1. (Enem / 2018) În mitologia greacă, Niobia era fiica lui Tantalus, două personaje cunoscute pentru suferința lor. Elementul chimic cu număr atomic (Z) egal cu 41 are proprietăți chimice și fizice atât de similare cu elementul cu numărul atomic 73 încât au fost confuzi.
Prin urmare, în cinstea acestor două personaje din mitologia greacă, acestor elemente li s-au dat numele de niobiu (Z = 41) și tantal (Z = 73). Aceste două elemente chimice au căpătat o mare importanță economică în metalurgie, în producția de supraconductori și în alte aplicații industriale de ultimă generație, tocmai datorită proprietăților chimice și fizice comun amândurora.
KEAN, S. Lingura care dispare: și alte povești adevărate despre nebunie, dragoste și moarte din elemente chimice. Rio de Janeiro: Zahar, 2011 (adaptat).
Importanța economică și tehnologică a acestor elemente, datorită similarității proprietăților lor chimice și fizice, se datorează
a) au electroni în subnivelul f.
b) fiind elemente de tranziție internă.
c) aparțin aceluiași grup de pe tabelul periodic.
d) au electronii lor cei mai exteriori la nivelurile 4 și respectiv 5.
e) să se afle în familia alcalino-pământului și respectiv alcalină.
Alternativă corectă: c) aparțin aceluiași grup din tabelul periodic.
Tabelul periodic este organizat în 18 grupe (familii), unde fiecare grup reunește elemente chimice cu proprietăți similare.
Aceste similitudini se întâmplă deoarece elementele unui grup au același număr de electroni în învelișul de valență.
Făcând distribuția electronică și adăugând electronii de la cel mai energetic subnivel la subnivelul cel mai exterior găsim grupul căruia îi aparțin cele două elemente.
| Niobiu | |
|
Distribuție Electronică |
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p65s2 4d3 |
|
suma de electroni |
mai energic + mai extern 4d3 + 5s2 = 5 electroni |
| grup | 5 |
| Tantal | |
|
Distribuție Electronică |
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f145d3 |
|
suma de electroni |
mai energic + mai extern 5d3 + 6s2 = 5 electroni |
| grup | 5 |
Elementele niobiu și tantal:
- Acestea aparțin aceluiași grup de pe tabelul periodic.
- Ei au electronii lor cei mai exteriori la nivelurile 5 și, respectiv, 6, așa că sunt localizați în perioada a 5-a și a 6-a.
- Au electroni în subnivelul d și, prin urmare, sunt elemente de tranziție în exterior.
2. (IFPE / 2018) Brazilia este cel mai mare producător de niob din lume, reprezentând peste 90% din rezerva acestui metal. Niobiul, simbolul Nb, este utilizat la producerea oțelurilor speciale și este unul dintre cele mai rezistente metale la coroziune și la temperaturi extreme. Compusul Nb2O5 este precursorul aproape tuturor aliajelor și compușilor niobiului. Bifați alternativa cu masa necesară de Nb2O5 pentru a obține 465 grame de niobiu. Dat: Nb = 93 g / mol și O = 16 g / mol.
a) 275 g
b) 330 g
c) 930 g
d) 465 g
e) 665 g
Alternativă corectă: e) 665 g
Compusul precursor al niobiului este oxidul de Nb2O5 iar niobiul utilizat în aliaje este sub forma elementară Nb.
Prin urmare, avem următoarea relație stoichiometrică:
1 mol de Nb2O5 generează 2 moli de Nb, deoarece oxidul de niobiu este format din 2 atomi ai acestui metal.
Pasul 1: calculați numărul de moli de niobiu produs care corespunde la 465 g.
Dacă prin calcul am văzut că masa niobiului corespunde cu 5 moli, atunci numărul de moli de Nb2O5 folosit este jumătate din această valoare, deoarece:
Al doilea pas: calculați masa molară a oxidului de niobiu.
Pasul 3: calculați masa de oxid de niobiu care corespunde la 2,5 moli.
3. (UECE / 2015) Brazilia deține 98% din rezervele mondiale de niobiu, care are numeroase aplicații industriale, cum ar fi fabricarea de bijuterii, implanturi hiperalergenice, electroceramice, magneți supraconductori, mașini cu rezonanță magnetică, aliaje metalice, monede speciale și în producția de oţel. Pentru niobiu, revedeți afirmațiile de mai jos și bifați singura alternativă adevărată.
a) Electronul său diferențial este situat în penultima coajă.
b) Este un element reprezentativ.
c) Electronegativitatea sa este mai mică decât cea a vanadiului.
d) Aparține celei de-a patra perioade a tabelului periodic.
Alternativă corectă: a) Electronul său diferențial este situat în penultimul înveliș.
Când se efectuează distribuția electronică a niobiului, este posibil să se vadă că electronul diferențial al acestuia se află în penultimul înveliș.
Deoarece are electronul diferențial în subnivelul d, este un element de tranziție exterior.
Deoarece nivelul său cel mai exterior se află în al cincilea strat, niobiul este situat în a cincea perioadă a tabelului.
Electronegativitatea este proprietatea legată de capacitatea elementului de a atrage electroni și variază în funcție de raza atomică: cu cât raza atomică este mai mică, cu atât este mai mare atracția pentru electroni și, prin urmare, cu atât este mai mare electronegativitate.
Consultând tabelul cu valorile electronegativității, este posibil să vedem că niobiul și vanadiul au valori apropiate de 1,6 Pauling.
4. (UEA / 2014) Izotopul natural al niobiului este 93Nb. Numărul de neutroni din acest izotop este
a) 41.
b) 52.
c) 93.
d) 134.
e) 144.
Alternativă corectă: b) 52.
Izotopii sunt atomi ai unui element chimic cu numere de masă diferite.
Masa atomică corespunde sumei protonilor și neutronilor unui element.
Numărul de protoni reprezintă numărul atomic al elementului chimic și pentru izotopi nu se modifică.
Astfel, variația masei izotopilor are loc datorită numărului diferit de neutroni.
Dacă numărul atomic de niobiu este 41, atunci numărul de neutroni este dat de calcul:
5. (IFMG / 2015) Elementul chimic niobiu, Nb, este numit după zeița greacă Niobe. Brazilia este cel mai mare producător mondial de metal, reprezentând 75% din producție. Datorită stabilității termice a aliajelor sale, niobiul este utilizat la producerea aliajelor speciale de oțel de înaltă rezistență pentru motoare, echipamente de propulsie și diverse materiale supraconductoare. Observând poziția niobiului pe tabelul periodic, este corect să afirmăm că:
a) cel mai energic subnivel va fi subnivelul d.
b) este un element aparținând familiei metalelor alcaline.
c) formează compuși ionici cu alte metale.
d) cationii săi vor avea o rază atomică mai mare decât elementul pur.
Alternativă corectă: a) cel mai energic subnivel va fi subnivelul d.
Privind tabelul periodic putem vedea că niobiul este caracterizat ca un element de tranziție exterior, care aparține grupului 5 al tabelului periodic, deoarece subnivelul său cel mai energetic este d.
Putem obține, de asemenea, aceste informații distribuindu-le electronic.
Deoarece este un metal, acest element face legături metalice cu alte metale, ca în aliaj legături fier-niobiu sau, de asemenea, covalente, prin împărțirea electronilor, ca în oxidul de niobiu Nb2O5.
6. (UFSC / 2003) Niobiul a fost descoperit în 1801, de către chimistul englez Charles Hatchett. Brazilia deține aproximativ 93% din producția mondială de concentrat de niobiu. Cele mai mari zăcăminte sunt situate în statele Minas Gerais, Goiás și Amazonas. Metalul este utilizat în principal la fabricarea aliajelor de fier-niobiu și a altor aliaje mai complexe, care au fost aplicate în construcția de turbine cu propulsie cu jet, rachete și nave spațiale. Oxizii săi sunt utilizați la fabricarea lentilelor ușoare pentru ochelari, camere fotografice și alte echipamente optice. Dat (Z = 41). În ceea ce privește niobiul, marcați propunerea (propunerile) CORECTĂ (e).
(01) Niobiul, atunci când pierde 3 electroni, își asumă configurația kriptonului.
(02) Niobiul poate forma oxizi metalici de tip M2O5 în2O3.
(04) Simbolul chimic pentru niobiu este Ni.
(08) Niobiul este un metal de tranziție.
(16) Un aliaj de fier-niobiu este un exemplu de soluție solidă.
Alternative corecte: 02 + 08 + 16 = 26.
(01) INCORECT.
| Elemente | Distribuție electronică |
| 36Kr | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 |
|
41Nb 41Nb3+ |
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d3 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 4p6 4d2 |
(02) CORECT
Având în vedere numerele de oxidare 3+ și 5+ pentru niobiu, acesta poate forma compușii:
| Numărul de oxidare 5+ | Numărul de oxidare 3+ |
| Nb2O5 | Nb2O3 |
(04) INCORECT
Ni este simbolul elementului nichel. Simbolul pentru niobiu este Nb.
(08) CORECT
Niobiul este un metal de tranziție extern aparținând grupei 5 din tabelul periodic.
(16) CORECT
O soluție solidă corespunde unui amestec de două sau mai multe componente în aceeași fază, care este solid, fiind obișnuit printre metale.
7. (UERJ / 2013) Niobiul este un metal care se găsește în depozite naturale, în principal sub formă de oxizi.
Într-un depozit care conține niobiu cu un număr de oxidare +5, formula pentru oxidul predominant al acestui metal corespunde:
a) NbO5
b) Nb5O
c) Nb5O2
d) Nb2O5
Alternativă corectă: d) Nb2O5
Oxigenul face două legături și are un număr fix de oxidare, care este 2-.
Prin urmare, pentru a forma oxid de niobiu, oxigenul trebuie să se lege de 2 atomi ai acestui metal.
Niobiul are stări de oxidare diferite. Cu numărul de oxidare 3+ se leagă de 3 oxigeni și cu Nox 5+ formează compusul: Nb2O5 în care 2 atomi de niobiu se leagă cu 5 atomi de oxigen.
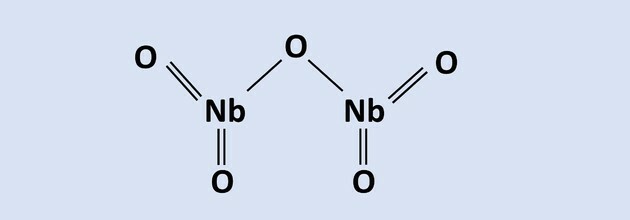
Citiți textul pentru a răspunde la întrebările 8-10.
Niobiul este un metal de mare importanță tehnologică, iar principalele sale rezerve mondiale sunt situate în
Brazilia, sub formă de minereu de piroclor, format din Nb2O5. Într-unul dintre procesele metalurgiei sale extractive, aluminotermia este utilizată în prezența oxidului de Fe2O3, rezultând un aliaj de niobiu și oxid de fier și aluminiu ca produs secundar. Reacția acestui proces este reprezentată în ecuația:
În natură, niobiul apare sub forma izotopului stabil niobiu-93, dar sunt cunoscuți mai mulți izotopi sintetici instabili, care se degradează prin emisia de radiații. Unul dintre ele este niobiu-95, care se descompune în elementul molibden-95.
(Systems.dnpm.gov.br; Tehnologie Metal. Mater. Miner., São Paulo, v. 6, nr. 4, p. 185-191, aprilie-iunie 2010 și G. Audi et al./Nuclear Physics A 729 (2003) 3–128. Adaptat)
8. (FGV / 2019) În reacția de aluminotermie pentru obținerea aliajului de niobiu și fier, având în vedere stoichiometria prezentată în ecuația echilibrată, numărul total de electroni implicați în proces este
a) 6.
b) 12.
c) 18.
d) 24.
e) 36.
Alternativă corectă: e) 36.
Reacția redox apare odată cu pierderea și câștigul de electroni.
Când un element reduce câștigă electroni și când un element este oxidat pierde electroni.
Atunci când un element îl reduce este un agent oxidant, în timp ce atunci când un element se oxidează este un agent reducător.
În acest fel, numărul de electroni care au fost pierduți de un element și dat la altul sunt egali.
| Element | NOX | Reacţie | electroni | |
| Niobiu |
+5 3Nb2O5 |
0 6Nb |
Reducere | 3.2.5 = 30 și- câștiguri |
| Fier |
+3 Credinţă2O3 |
0 2Fe |
Reducere | 2.3 = 6 și- câștiguri |
| Aluminiu |
0 12Al |
+3 6Al2O3 |
Oxidare | 6.2.3 = 36 și- pierdut |
Sarcina de aluminiu pe produsul cu oxid de aluminiu este de 3+, adică fiecare aluminiu a pierdut 3 electroni.
Dar în produse avem 12 atomi de aluminiu, ceea ce face ca numărul total de electroni implicați în proces:
12. 3 = 36 electroni.
9. (FGV / 2019) Într-o operație de aluminotermie pentru producția de niobiu și aliaj de fier cu cantități stoichiometrice de Nb2O5 și Fe2O3 și utilizarea excesului de aluminiu metalic, s-au format 6,12 tone de Al.2O3. Suma totală a cantităților, în moli, de niobiu și fier estimată a fi obținută în această operație este
a) 6 × 104
b) 6 × 106
c) 8 × 103
d) 8 × 104
e) 8 × 106
Alternativă corectă: d) 8 × 104.
Pasul 1: calculați masa molară a lui Al2O3
Al doilea pas: calculați numărul de moli de Al2O3
Pasul 3: efectuați relațiile stoichiometrice.
În ecuația chimică, vedem că există relația: 6 moli de niobiu, 6 moli de aluminiu și 2 moli de fier.
După raportul numărului de moli formați, avem:
Iar suma cantităților de niobiu și fier, în moli, este:
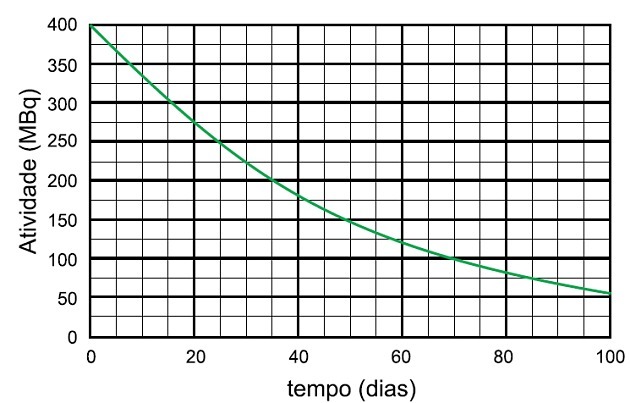
În procesul de dezintegrare a radioizotopului niobiu-95, timpul necesar pentru ca această probă să se descompună la 25 MBq și numele speciei emise sunt
a) 140 de zile și neutroni.
b) 140 de zile și protoni.
c) 120 de zile și protoni.
d) 120 de zile și particule ß–.
e) 140 de zile și particule ß–.
Alternativă corectă: e) 140 de zile și particule ß–.
Timpul de înjumătățire este timpul necesar unui eșantion radioactiv pentru a-și înjumătăți activitatea.
În grafic vedem că activitatea radioactivă începe la 400 MBq, deci timpul de înjumătățire este timpul necesar pentru ca activitatea să se descompună la 200 MBq, care este jumătate din cea inițială.
Analizăm în grafic că de data aceasta a fost de 35 de zile.
Pentru ca activitatea să scadă din nou la jumătate, au trecut alte 35 de zile și activitatea a trecut de la 200 MBq la 100 MBq când au trecut alte 35 de zile, adică de la 400 la 100 MBq au trecut 70 de zile.
Pentru ca proba să se descompună până la 25 MBq, au fost necesare 4 timpi de înjumătățire.
Ceea ce corespunde:
4 x 35 de zile = 140 de zile
În decăderea radioactivă, emisiile pot fi alfa, beta sau gamma.
Radiația gamma este o undă electromagnetică.
Emisia alfa are o sarcină pozitivă și scade 4 unități în masă și 2 unități în numărul atomic al elementului descompus, transformându-l într-un alt element.
Emisia beta este un electron de mare viteză care crește numărul atomic al elementului descompus cu o unitate, transformându-l într-un alt element.
Niobiu-95 și molibden-95 au aceeași masă, deci s-a produs o emisie beta deoarece: