O raza atomica elementelor este o proprietate periodică care determină raza unui atom care variază în funcție de poziția elementului în tabelul periodic.
Astfel, pot crește și scădea pe măsură ce numar atomic (Z) al elementului care corespunde numărului de protoni prezenți în nucleul atomilor.
Pe scurt, raza atomică corespunde cu jumătate din distanța dintre nucleele a doi atomi vecini, fiind exprimată după cum urmează:
r = d / 2
de unde:
r = raza
d = distanță internucleară
În general, raza atomică este măsurată în picometre (pm), sub-multiplu al contorului (1 picometru = 10-12 m.). Rețineți că atunci când referința nu este un atom, ci un ion, raza găsită este raza ionică.
Variația razei atomice
În tabelul periodic, creșterea razei atomice poate fi văzută în următoarea figură:
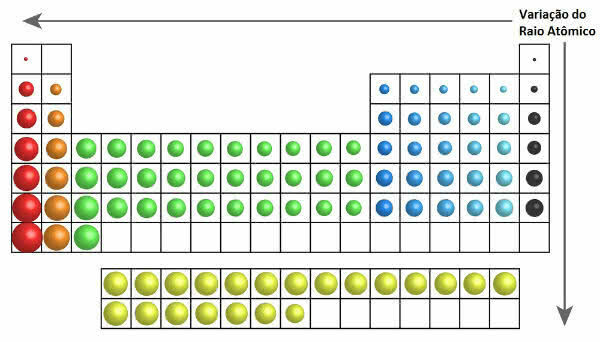 Variația razei atomice în tabelul periodic
Variația razei atomice în tabelul periodic
Astfel, pe verticală (familii sau grupuri) raza atomică crește de sus în jos. Pe orizontală (puncte), ele cresc de la dreapta la stânga.
Vedeți variația inversă în Afinitate electronică și electronegativitate.
Energie de ionizare
THE energie (sau potențial) de ionizare este, de asemenea, o proprietate periodică care determină energia necesară pentru deplasarea unui electron, care este exprimată în electroni volți (eV).
Citește și: Proprietăți periodice.
Verificați întrebările la examenul de admitere cu o rezoluție comentată în: Exerciții pe tabelul periodic.



