O princip Le Chateliera govori nam da će se, kada je poremećaj uzrokovan u sustavu u ravnoteži, pomaknuti u smjeru koji umanjuje sile stvorene tim poremećajem i uspostavlja novu kemijsku ravnotežu.
Jedna od tih smetnji je i varijacija temperature. Ova je varijacija važna jer će, osim što će uzrokovati pomak ravnoteže, promijeniti i vrijednost konstante ravnoteže, Kç.
Da biste bolje razumjeli kako se to događa, pogledajmo primjer:
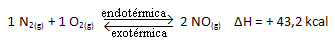
Kç = _ [U]2___
[N2]. [O.2]
Gornja reakcija događa se u izravnom smjeru s apsorpcijom energije, endotermna je. Obrnuti se proces, pak, događa s oslobađanjem energije, što je egzotermna reakcija.
Dakle, ako povećamo temperaturu sustava, kemijska će se ravnoteža pomaknuti prema endotermnoj reakciji, koja je u ovoj reakciji udesno. To je tako da se toplina apsorbira i uspostavi ravnoteža.
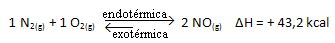
Tačno je i suprotno; ako snizimo temperaturu ovog sustava, reakcija će se pomaknuti u smjeru u kojem će oslobađati toplinu, jer će se ukupna energija reakcije smanjivati. To znači da će se ravnoteža pomaknuti prema egzotermnoj reakciji, koja je u ovom slučaju slijeva:
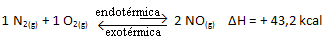
Ukratko:

U odnosu na konstantu ravnoteže (Kç), kada se temperatura povećava, favorizira endotermnu reakciju i više NO(g) nastaje povećavajući njegovu koncentraciju i smanjujući koncentraciju reaktanata. U donjoj formuli imajte na umu da je koncentracija NO(g) je izravno proporcionalan konstanti Kç, stoga se također povećava:
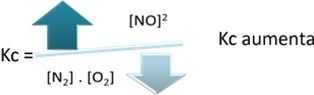
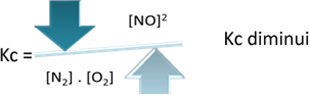
Ali ako smanjimo temperaturu, prebacujući reakciju prema egzotermnoj reakciji, koncentracija NO produkta će se smanjiti, a koncentracije reaktanata će se povećati. Budući da su koncentracije reaktanata obrnuto proporcionalne konstanti Kc, tada će se smanjivati:
Napisala Jennifer Fogaça
Diplomirao kemiju
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/variacao-temperatura-deslocamento-equilibrio-quimico.htm

