THE isomerismi se on ilmiö, joka havaitaan, kun samantyyppisiä atomeja muodostaa eri yhdisteitä yhtä suuresta määrästä.
Siksi voimme löytää kemiallisia aineita, joilla on sama molekyylikaava ja erilaiset rakennekaavat tai tilajärjestelyt.
Tämä ilmiö havaitaan laajalti orgaanisessa kemiassa, joka tutkii hiiliyhdisteitä. Koska jokainen tämän alkuaineen atomi voi muodostaa 4 kemiallista sidosta, on mahdollista havaita erilaisia yhdistelmiä.
Koska atomien järjestelyn muutos synnyttää uusia aineita, niillä on erilaisia fysikaalisia ja kemiallisia ominaisuuksia.
Kun sanomme, mitkä yhdisteet ovat isomeerit tarkoittaa, että niillä on yhtä suuret osat, koska sana on yhdistelmä kahdesta kreikkalaista alkuperää olevasta termistä: isos, tarkoittaa "todella" ja pelkkä, joka on "osat".
Isomerismin kaksi pääryhmää ovat taso ja avaruus (stereoisomerismi).
THE tasainen isomeria se voidaan visualisoida yhdisteiden litteällä rakennekaavalla, ja sillä on viisi luokkaa: sijainti, toiminta, ketju, kompensaatio ja tautomeeri.
THE avaruuden isomerismi se havaitaan yhdisteiden orientaation perusteella ja se jaetaan geometriseen (cis-trans) ja optiseen.
Isomerian käsitteen esitteli vuonna 1830 ruotsalainen tiedemies Jacob Berzelius.
Esimerkkejä isomeereistä
THE ketjun isomeria se tapahtuu, kun sama atomisarja yhdistyy muodostaen saman funktionaalisen ryhmän rakenteita, mutta eri ketjuilla.
Esimerkki: molekyylikaava C4H10 hiilivety voi olla suora tai haarautunut.

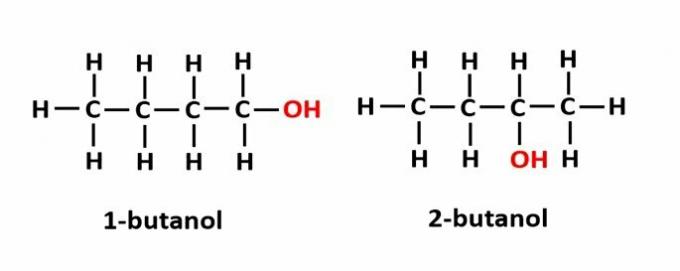
THE asema-isomeria tapahtuu, kun yhdisteet muodostuvat samoista funktionaalisista ryhmistä, mutta ne ovat ketjun eri kohdissa.
Esimerkki: Molekyylikaava C4H9OH vastaa kahta alkoholityyppiä.
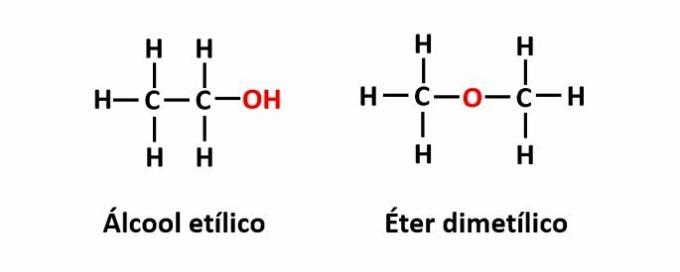
THE funktion isomeria tapahtuu, kun sama molekyylikaava vastaa kahta yhdistettä, joissa on eri funktionaalisia ryhmiä.
Esimerkki: Molekyylikaava C2H6O vastaa kahta isomeeriä, joilla on alkoholi (-OH) ja eetteri (-O-) funktio.
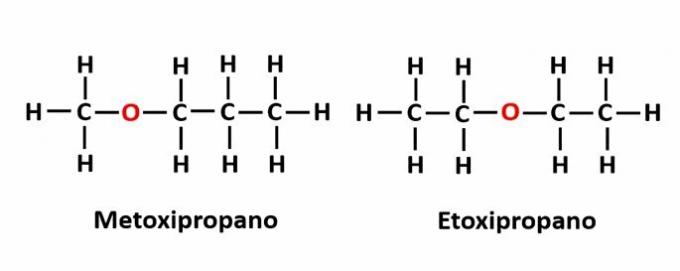
THE kompensaatioisomeria se tapahtuu, kun ketjussa on heteroatomi ja se on eri asemissa. Tämä on erityinen paikka-isomerian tapaus.
Esimerkki: Molekyylikaava C4H10Merkki osoittaa happiatomin läsnäolon ketjussa, mutta sen sijainti voi muuttua ja muodostaa erilaisia yhdisteitä.
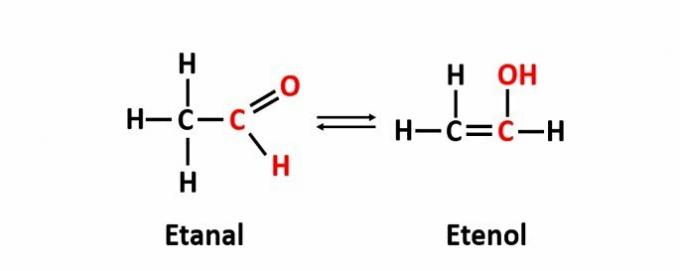
THE dynaaminen isomeria, jota kutsutaan myös tautomeeriksi, tapahtuu, kun kaksi yhdistettä, joilla on eri toiminnot, ovat samassa liuoksessa dynaamisessa tasapainossa. Tämä on erityinen funktio-isomerian tapaus.
Esimerkki: Molekyylikaava C2H4O vastaa yhdisteitä, joissa on aldehydi- ja enolifunktioita.
Lisätietoja: tasainen isomeria.
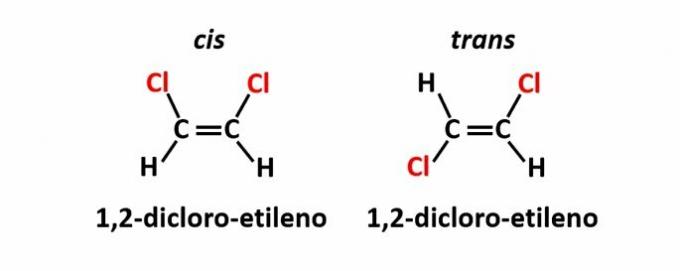
THE geometrinen isomeria, jota kutsutaan myös isomeeriksi cis-trans, tapahtuu, kun kaksoissidoksen tai syklisen rakenteen läsnäolo saa samanlaiset ligandit olemaan samalla puolella tasoa (IVY) tai vastakkaisilla puolilla (trans).
Esimerkki: klooriatomit yhdisteissä, joilla on molekyylikaava C2H2Cl2 niillä voi olla kaksi tilarakennetta.
THE optinen isomeria tapahtuu, kun rakenteeseen säteilevää polarisoitua valoa kääntäessään yhdisteet onnistuvat kääntämään säteen valoa vasemmalle, jos se on vasemmalle kiertävä (l) isomeeri, tai oikealle, kun se on oikealle kiertävä isomeeri (d).
Esimerkki: Tämän tyyppistä isomeriaa esiintyy maitohapon kanssa. Huomaa alla, että isomeerien spektrikuvat eivät mene päällekkäin, joten niitä kutsutaan enantiomeereiksi.
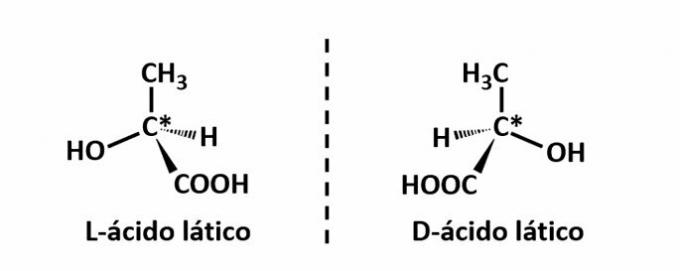
Symboli C* osoittaa kiraalisen hiilen läsnäolon tässä rakenteessa, eli hiiliatomin, jossa on 4 erilaista linkkeriä.
Lisätietoja isomeriasta sisällön kanssa:
- Isomerian tyypit
- avaruuden isomeeri
- geometrinen isomeeri
- optinen isomeeri
- Harjoituksia tasoisomeriasta



