Löslichkeit ist die physikalische Eigenschaft von Stoffen, sich in einer bestimmten Flüssigkeit aufzulösen oder nicht.
wird genannt gelöst, chemische Verbindungen, die sich in einer anderen Substanz auflösen. Ö Lösungsmittel es ist die Substanz, in der der gelöste Stoff aufgelöst wird, um ein neues Produkt zu bilden.
DAS chemische Auflösung ist der Vorgang des Dispergierens des gelösten Stoffes in einem Lösungsmittel, wodurch eine homogene Lösung oder Mischung entsteht.
Gelöste Stoffe können unterteilt werden in:
- Löslich: sind die gelösten Stoffe, die sich im Lösungsmittel lösen.
- Schwach löslich: sind die gelösten Stoffe, die im Lösungsmittel schwer löslich sind.
- Unlöslich: sind die gelösten Stoffe, die sich nicht im Lösungsmittel lösen.
Ein gängiges Prinzip bei der Löslichkeit ist: "wie auflösen wie”. Dies bedeutet, dass ein polarer gelöster Stoff dazu neigt, sich in einem polaren Lösungsmittel aufzulösen. Das gleiche gilt für unpolare Stoffe.
Sehen Sie einige Beispiele:
- Kohlenwasserstoffe, im Benzin enthaltene Verbindungen, sind unpolar und haben eine geringe Löslichkeit in Wasser, das polar ist.
- Alkohole wie Ethanol und Methanol sind aufgrund des Vorhandenseins von Sauerstoff in der Kohlenstoffkette polar und daher in Wasser löslich.
- Salze haben unterschiedliche Löslichkeiten. Sie können unterteilt werden in: lösliches Salz und praktisch unlösliches Salz.
Löslichkeitskoeffizient
Ö Löslichkeitskoeffizient (Cs) bestimmt die maximale Kapazität des gelösten Stoffes, der sich in einer bestimmten Lösungsmittelmenge löst. Dies ist abhängig von den Temperaturbedingungen.
Zusammenfassend ist der Löslichkeitskoeffizient die Menge an gelöstem Stoff, die benötigt wird, um eine Standardmenge an Lösungsmittel unter einer gegebenen Bedingung zu sättigen.
Betrachten Sie beispielsweise die folgende Situation:
In einem Glas Salzwasser (NaCl) verschwindet das Salz zunächst im Wasser.
Wenn jedoch mehr Salz hinzugefügt wird, beginnt es sich irgendwann am Boden des Glases anzusammeln.
Dies liegt daran, dass das Wasser als Lösungsmittel seine Löslichkeitsgrenze und die maximale Konzentration erreicht hat. Das nennt man auch Sättigungspunkt.
Der gelöste Stoff, der am Boden des Behälters verbleibt und sich nicht auflöst, wird als Bodenkörper oder Niederschlag bezeichnet.
Im Verhältnis zu Sättigungspunkt, werden die Lösungen in drei Typen eingeteilt:
- ungesättigte Lösung: wenn die Menge an gelöstem Stoff weniger als Cs beträgt.
- gesättigte Lösung: wenn die Menge des gelösten Stoffes genau der von Cs entspricht. Es ist die Sättigungsgrenze.
- übersättigte Lösung: wenn die Menge des gelösten Stoffes größer als Cs ist.
Löslichkeitsprodukt
Wie wir gesehen haben, repräsentiert die Löslichkeit die Menge des gelösten Stoffes in einer Lösung. Ö Löslichkeitsprodukt (Kps) ist eine Gleichgewichtskonstante, die sich direkt auf die Löslichkeit bezieht.
Mit seiner Berechnung können Sie feststellen, ob eine Lösung gesättigt, ungesättigt oder mit einem Niederschlag gesättigt ist. Diese Berechnung bezieht sich auf das Auflösungsgleichgewicht und die Konzentration der Ionen in der Lösung.
Dies liegt daran, dass sich das Löslichkeitsprodukt auf das Auflösungsgleichgewicht ionischer Substanzen bezieht.
mehr über verstehen Gelöste und Lösungsmittel.
Löslichkeitskurve
Die chemische Löslichkeit eines Stoffes, der einer Temperaturänderung ausgesetzt ist, ist nicht linear. Die Veränderung der Löslichkeitskapazität in Abhängigkeit von der Temperatur wird als Löslichkeitskurve bezeichnet.
Der Löslichkeitskoeffizient der meisten Feststoffe nimmt mit steigender Temperatur zu. Somit stellt sich die Löslichkeit jedes Materials proportional zur Temperatur ein.
Jeder Stoff hat seine eigene Löslichkeitskurve für ein bestimmtes Lösungsmittel.
Die Löslichkeitsvariation wird als linear betrachtet, wenn sie nicht unter Temperatureinfluss steht. Um die Variation zu kennen, ist es notwendig, die Löslichkeitskurve zu betrachten.
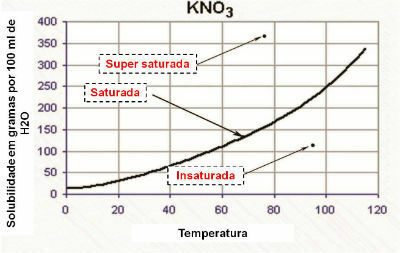
Löslichkeitskurve
In der Grafik zeigt die Löslichkeitskurve, dass die Lösung ist:
- gesättigt: wenn der Punkt auf der Löslichkeitskurve liegt.
- ungesättigt: wenn der Punkt unterhalb der Löslichkeitskurve liegt.
- homogen gesättigt: wenn der Punkt über der Löslichkeitskurve liegt.
Lesen Sie auch über Lösungskonzentration.
Löslichkeitskoeffizient-Formel
Die Formel zur Berechnung des Löslichkeitskoeffizienten lautet:
Cs = 100. ich1/m2
Wo:
Cs: Löslichkeitskoeffizient
ich1: Masse des gelösten Stoffes
ich2: Lösungsmittelmasse
Möchten Sie mehr wissen? lesen Chemische Lösungen und Verdünnung von Lösungen.
Übungen
1. (Fuvest-SP) Ein Chemiker las die folgende Anweisung in einem Verfahren, das in seinem Laborhandbuch beschrieben ist:
"Löse 5,0 g Chlorid in 100 ml Wasser bei Raumtemperatur auf..." .
Welcher der folgenden Stoffe wird im Text erwähnt?
a) Cl2.
b) CCl4.
c) NaClO.
d) NH4Kl.
e) AgCl.
d) NH4Kl.
2. (UFRGS-RS) Ein bestimmtes Salz hat eine Wasserlöslichkeit von 135 g/L bei 25°C. Durch vollständiges Auflösen von 150 g dieses Salzes in einem Liter Wasser bei 40 °C und langsames Abkühlen des Systems auf 25 °C wird ein homogenes System erhalten, dessen Lösung:
a) verdünnt.
b) konzentriert.
c) ungesättigt.
d) gesättigt.
e) übersättigt.
e) übersättigt.
3. (Mackenzie-SP) Ein typisches Beispiel für eine übersättigte Lösung ist:
Das Mineral Wasser.
b) hausgemachtes Serum.
c) Soda in einem geschlossenen Behälter.
d) Alkohol 46° GL.
e) Essig.
c) Soda in einem geschlossenen Behälter.
4. (PUC-RJ) Beachten Sie die folgende Abbildung, die die Löslichkeit in g pro 100 g H2O von 3 anorganischen Salzen in einem bestimmten Temperaturbereich darstellt:
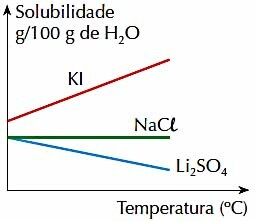
Überprüfen Sie die richtige Aussage:
a) Die Löslichkeit der 3 Salze nimmt mit der Temperatur zu.
b) Die Temperaturerhöhung begünstigt die Solubilisierung von Li2NUR4.
c) Die Löslichkeit von KI ist im angegebenen Temperaturbereich größer als die Löslichkeiten anderer Salze.
d) Die Löslichkeit von NaCl variiert mit der Temperatur.
e) Die Löslichkeit von 2 Salzen nimmt mit der Temperatur ab.
c) Die Löslichkeit von KI ist im angegebenen Temperaturbereich größer als die Löslichkeiten anderer Salze.