Sie nennen sich selbst innere Übergangselemente alle 28 chemische Elemente in der 6. und 7. Periode der Gruppe 3 (oder der Familie IIIB) der Periodensystem. Sie sind genauer außerhalb des Hauptteils der Tabelle positioniert.
werden genannt Übergangselemente weil sie nicht zu den Familien A (repräsentative Elemente) gehören, aber nicht mit den Elementen verwechselt werden können des externen Übergangs (Elemente, die zu den Familien B gehören und im Hauptteil der Tabelle positioniert sind periodisch).
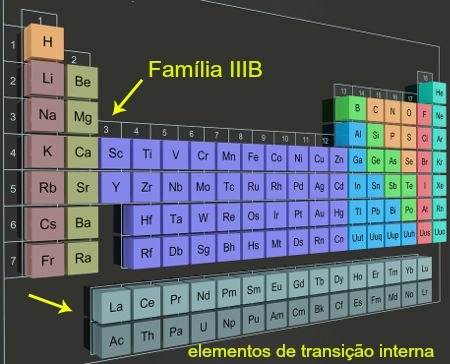
Interne Übergangselemente in Spalten außerhalb des Periodensystems
Sie innere Übergangselemente präsentieren die Unterebene f als energischer. Ein Beweis dafür ist, dass jede der horizontalen Spalten, die sich auf diese Elemente beziehen, nur 14 Elemente hat, wobei 14 die maximale Anzahl von Elektronen unterstützt durch Unterebene f.
a) Lanthanoid-Reihe
Die Lanthanoide sind alle diejenigen, die ausschließlich zur 6. Periode der IIIB-Familie gehören und so genannt werden, weil das erste Element in der Reihe Lanthan (La) ist. Sehen Sie sich die Namen und Akronyme von allen an:
Lanthan (La)
Cer (C)
Praseodym (Pr)
Neodym (Nd)
Promethium (PM)
Samarium (Sm)
Europium (I)
Gadolinium (Gd)
Terbium (Tb)
Dysprosium (Dy)
Holmium (Ho)
Erbium (Er)
Thulium (Tm)
Ytterbium (Yb)
Alle internen Übergangselemente präsentieren die 4f-Unterebene als die energiereichste, d elektronische Verteilung von allen endet auf dieser Unterebene, wie wir an der Verteilung von zwei Elementen der Reihe sehen können:
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
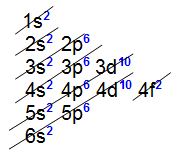
Elektronische Verteilung des Lanthanoid-Elements Cerium

Elektronische Verteilung des Lanthanoid-Elements Holmium
b) Actiniden-Reihe
Aktinide sind alle diejenigen, die ausschließlich zur 7. Periode der IIIB-Familie gehören und so genannt werden, weil das erste Element in der Reihe Actinium (Ac) ist. Sehen Sie sich die Namen und Akronyme von allen an:
Aktinium (Ac)
Thorium (Do)
Protactinium (Pa)
Uran (U)
Neptunium (Np)
Plutonium (Pu)
Americium (Am)
Curium (cm)
Berkelium (Bk)
Kalifornien (vgl.)
Einsteinium(e)
Fermium (Fm)
Mendelevium (Md)
Nobel (Anm.)
Alle internen Übergangselemente stellen die 5f-Unterebene als die energiereichste dar, d. h. die Verteilung Elektronik von allen endet auf dieser Unterebene, wie wir an der Verteilung zweier Elemente sehen können, die zu gehören die Serie:

Elektronische Verteilung des Uran-Actiniden-Elements

Elektronische Verteilung des kalifornischen Aktinidenelements
Von mir. Diogo Lopes Dias
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
TAGE, Diogo Lopes. "Interne Übergangselemente"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/elementos-transicao-interna.htm. Zugriff am 27. Juni 2021.

