Beim Moleküle es handelt sich um Strukturen mit einer bestimmten Molmasse und einer relativ kleinen und genauen Anzahl von Atomen, die kovalent, d. h. durch die gemeinsame Nutzung von Elektronen, miteinander verbunden sind.
Siehe drei Beispiele:
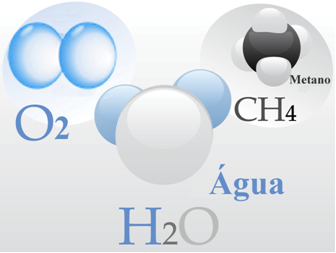
- Sauerstoffgas: Seine Moleküle werden jeweils durch eine Doppelbindung gebildet, d. h. durch die gemeinsame Nutzung zweier Elektronenpaare zwischen zwei Sauerstoffatomen (O2);
- Wasser: es wird von H-Molekülen gebildet2Ö. Das bedeutet, dass jedes Molekül zwei Wasserstoffatome hat, die sich ein Elektronenpaar mit jeweils einem Sauerstoffatom teilen.
- Methan: diese Verbindung wird von CH-Molekülen gebildet4, in der vier Wasserstoffatome kovalent an ein Kohlenstoffatom binden.
Molekulare Substanzen haben einige charakteristische Eigenschaften, wie zum Beispiel:
- Unterschiedliche Löslichkeit in Wasser und anderen Lösungsmitteln;
- Sie können sich in den drei physikalischen Zuständen präsentieren;
- Im Allgemeinen handelt es sich um elektrische Isolatoren, sowohl fest als auch flüssig.
Alle Moleküle werden von nichtmetallischen Elementen gebildet, dh sie enthalten nur Wasserstoff, Nichtmetalle und Halbmetalle. Diese Elemente können aber auch Stoffe bilden, die nur im festen Zustand vorliegen und die ganz andere Eigenschaften haben als Moleküle. Dies sind die Makromoleküle.
Makromoleküle, auch bekannt als kovalente Feststoffe oder kovalente Netzwerkkörper,sie sind Strukturen mit einer sehr hohen und ungenauen Molmasse, zusätzlich dazu, dass sie aus einer großen und unbestimmten Menge von Atomen bestehen, die sich kovalent zu dreidimensionalen Gittern verbinden. Die Makromoleküle bilden die kovalente Kristalle oder Atomkristalle.
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Zum Beispiel können Kohlenstoffatome Elektronen auf viele Arten teilen und viele verschiedene einfache Substanzen bilden. Diese Eigenschaft, dass dasselbe chemische Element zwei oder mehr verschiedene einfache Stoffe bilden muss, wird als. bezeichnet Allotropie.
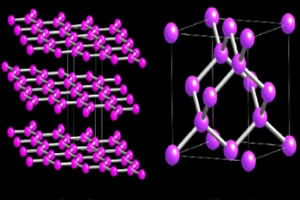
Zwei allotrope Kohlenstoffarten, die Makromoleküle bilden, sind die Diamant und der Graphit. In den Bildern unten sehen Sie, dass bei Diamant jedes Kohlenstoffatom an vier weitere Kohlenstoffatome bindet und ein Makromolekül mit tetraedrischer Struktur entsteht.

Inzwischen wird die Graphitstruktur durch hexagonale Ringe gebildet, die in derselben Ebene enthalten sind. Kohlenstoffatome bilden eine Doppel- und zwei Einfachbindungen.

Aber Makromoleküle bestehen nicht nur aus einem einzigen Elementtyp; sie können auch aus Atomen verschiedener chemischer Elemente gebildet werden.
Ein Beispiel ist Siliziumdioxid (Quarz), dessen Makromoleküle jedes Siliziumatom von vier Kohlenstoffatomen umgeben und jedes Sauerstoffatom mit zwei Siliziumatomen verbunden ist.
Von Jennifer Fogaça
Abschluss in Chemie
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
FOGAÇA, Jennifer Rocha Vargas. "Moleküle und Makromoleküle"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/moleculas-macromoleculas.htm. Zugriff am 28. Juni 2021.
Chemie
Was ist Allotropie, einfache Substanzen, Gassauerstoff, Ozon, allotrope Formen, chemisches Element Sauerstoff, ultraviolette Strahlen der Sonne, Diamant, Graphit, Atomarität, weißer Phosphor.
Raumformel von Kohlenstoff, elektronische Formel von Lewis, ebene Struktur, elektronische Paare, Bindung kovalent, Valenzschicht, Evolution des Atommodells, Summenformel, Strukturformel, Formeln dreidimensional.
Chemische Formeln, flache Strukturformel, Couper-Strukturformel, Dreifachbindung, Gas Stickstoff, elektronische Formel, Lewis-Formel, Summenformel, Einfachbindung, Doppelbindung, Gas Kohlensäure.



