Ein Molekül ist eine Gruppe von Atomen gleicher oder verschiedener Elemente. Sehen Sie einige Beispiele:
H2Ö – Molekül, das aus zwei verschiedenen Elementen besteht (zwei Wasserstoffatome und ein Sauerstoffatom);
Cl2– Molekül, das nur aus einem einzigen chemischen Element (zwei Chloratomen) besteht.
Beim Moleküle kann eingeteilt werden in Polar- oder apolar:
unpolar: Moleküle ohne Pole (positiv und negativ);
Polar-: Moleküle, die Pole haben (positiv und negativ).
In diesem Text betonen wir die polare Moleküle. Um a zu identifizieren polares Molekül, Wir können eine der folgenden vorgeschlagenen Strategien verwenden:
Das) ionische Verbindung (durch Ionenbindung gebildet)
Wenn der Stoff stammt von Ionenverbindung (zwischen einem Metall und einem Nichtmetall) bedeutet, dass es von Ionen (Kation und Anion) gebildet wird. Daher präsentiert sich dieser Stoff automatisch polare Moleküle, da Ionen positive und negative Ladungen haben.
Beispiele:
NaCl (Na ist ein Metall und Cl ist ein Nichtmetall);
CaO (Ca ist ein Metall und O ist ein Nichtmetall);
MgS (Mg ist ein Metall und S ist ein Nichtmetall).
B) Molekulare Verbindungen (gebildet durch kovalente Bindung)
Wenn die Verbindung molekular ist, müssen wir jeden Fall analysieren, da wir die Möglichkeit haben, mehrere verschiedene Moleküle zu haben. Im Folgenden sind einige Beispiele und Regeln aufgeführt, die bei der Bestimmung polarer Molekülverbindungen hilfreich sein können:
- Zweiatomiges Molekül mit verschiedenen Elementen
Wenn die molekulare Verbindung nur aus zwei Atomen besteht und diese beiden Atome aus verschiedenen Elementen bestehen, automatisch ist das Molekül polar, weil die beiden Atome unterschiedliche Elektronegativitäten haben. Beispiele: HBr und NO.
- Moleküle mit zwei oder mehr Atomen (gleich oder anders)
Bei Molekülen mit mehr als zwei Atomen müssen wir die Menge der Wolken berücksichtigen Binder und Nichtbinder, die im Zentralatom des Moleküls vorhanden sind, und vergleiche es mit der Anzahl gleicher Atome, die an das Atom gebunden sind zentral. Die Bindungswolken sind Einfachbindungen (ein Elektron aus der Valenzschale jedes beteiligten Atoms), Doppelbindungen (zwei Elektronen aus der Valenzschale jedes beteiligten Atoms) oder Tripel (drei Elektronen aus der Valenzschale jedes Atoms) beteiligt). Die nicht bindenden Wolken sind die Elektronenpaare in der Valenzschale, die nicht an den Bindungen teilnehmen.
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Überwachung: Um die Anzahl der Elektronen in der Valenzschale eines bestimmten Atoms zu kennen, muss man nur seine Periodenfamilie kennen:

Um festzustellen, ob das Molekül polar ist, genügt es zu prüfen, ob sich die Anzahl der im Zentralatom vorhandenen Wolken von der Anzahl der daran gebundenen gleichen Atome unterscheidet. Sehen Sie einige Beispiele:
HCN
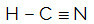
Das Zentralatom des Moleküls ist Kohlenstoff und hat zwei verschiedene Bindemittel,zwei bindende Wolken (einfach und dreifach) und kein Paar nichtbindender Elektronen (es stammt aus der VIA-Familie, es hat vier Elektronen in der Valenzschale und verwendet alle vier, eines in der Einfachbindung und drei im Dreifach). Aus diesem Grund bildet es ein polares Molekül.
Zusamenfassend:
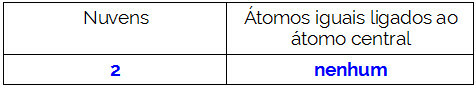
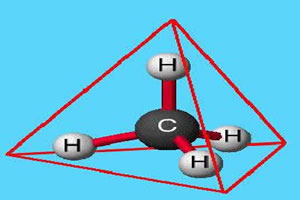
NH3
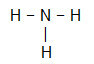
Das Zentralatom des Moleküls ist Stickstoff und hat drei gleiche Liganden und insgesamt vier Wolken, drei bindende Wolken (drei Einfachbindungen) und eine nichtbindende (sie stammt aus der VA-Familie, sie hat fünf Elektronen) in der Valenzschicht und verwendet nur drei, eine in jeder einzelnen Verbindung, so dass zwei nicht Bindemittel).
Aus diesem Grund ist das Zentralatom von NH3 bildet ein polares Molekül.
Zusamenfassend:

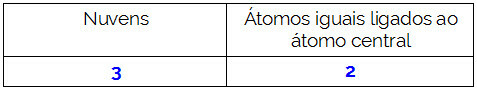
CH2Ö
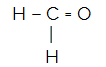
Das Zentralatom des Moleküls ist Kohlenstoff und hat zwei identische und einen unterschiedlichen Liganden, sowiedrei bindende Wolken (zwei Einfach- und eine Doppelbindung), kein Paar nichtbindender Elektronen (es ist aus der VIA-Familie, es hat vier Elektronen in der Valenzschale und nutzt die 4, zwei in den Singles und zwei in der Paar). Aus diesem Grund bildet es ein polares Molekül.
Zusamenfassend:
Von mir. Diogo Lopes Dias
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
TAGE, Diogo Lopes. "Polare Moleküle"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/moleculas-polares.htm. Zugriff am 28. Juni 2021.
Ionische Verbindungen, Hauptmerkmale ionischer Verbindungen, Bindung zwischen Ionen, definitive Übertragung von Elektronen, elektrostatische Anziehungskräfte zwischen Ionen, negativen und positiven Ionen, Anionen, Kationen, Ionenbindung, Molekülstruktur er
Chemie
Molekulare Stoffe, Siedetemperatur, Kontaktfläche, Siedepunkt, intermolekulare Anziehungskräfte, chemische Bindung, molekulare Verbindungen, kovalente chemische Bindungen, ionische Bindungen, metallische Bindungen, Aggregatzustände von Schlecht
