Salzsäure ist eine Wassersäure mit hohem Ionisationspotential, es ist eine gelbliche Flüssigkeit, stark ätzend und giftig. Es wird in verschiedenen industriellen Prozessen wie der Herstellung von Reinigungsmitteln und pharmazeutischen Hydrochloriden, in Lebensmitteln und in Stahlherstellungsprozessen verwendet.
Es ist auch im menschlichen Organismus vorhanden; Ö Magensäure die bei der Verdauung von wirkt Proteine eine saure Lösung ist; von Salzsäure und anderen Stoffen, wie z Enzyme und Salze. Exposition, Einatmen oder Verschlucken von konzentrierte Salzsäure ist hoch gesundheitsschädlich, die sogar zum Tod führen können.
Lesen Sie auch: Schwefelsäure - Substanz mit hoher Korrosionskraft
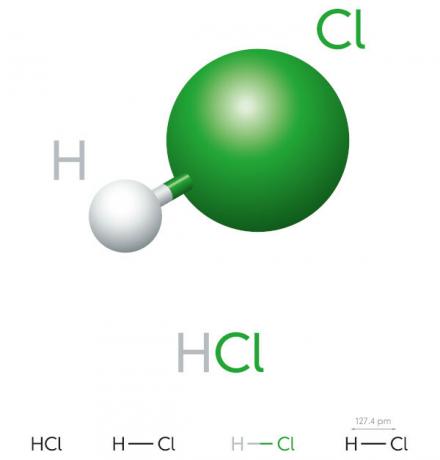
Salzsäure-Eigenschaften
- anorganische Verbindung
- starke Säure
- Hohes Ionisationspotential
- Flüssigkeit
- gelbliches Aussehen
- Giftig
- Ätzend
- Flüchtig
- Hygroskopisch (eigentlich zu absorbieren áWasser der Umwelt)
- In Wasser löslich
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Salzsäureherstellung
Die Salzsäure war von einem muslimischen Alchemisten entdeckt genannt Jabir Ibne Haiane, auch bekannt als Gaber und gilt als der Vater der arabischen Chemie. Er synthetisierte die Substanz basierend auf a Reaktion zwischen Meersalz (NaCl) und dem Schwefelsäure (Beim2NUR4).
2NaCl + H2NUR4 → In2NUR4 + 2HCl
Derzeit Salzsäure wird in großem Umfang durch die elektronischóLyse Natriumchlorid in wässriger Lösung. Aus diesem Prozess wird Gas gewonnen Chlor (Cl2), Gas Wasserstoff (H2) und Natriumhydroxid (NaOH). Chlor- und Wasserstoffgase reagieren zu Salzsäure:
Cl2 + H2 → 2HCl
Jedoch, diese Reaktion ist extrem exotherm und hochgefährlich. Gegenwärtig wird der größte Teil der industriell hergestellten Salzsäure mit der Herstellung organischer Verbindungen in Verbindung gebracht, die ein wirtschaftlicheres und sichereres Verfahren darstellt.
R-H + Cl2 → R-Cl + HCl
(Betrachten Sie R als organisches Radikal.)
Auch sehen: Tipps zur Bestimmung-wenn die Stärke der Säuren

Anwendung von Salzsäure
- Metallbeizen: Salzsäure wird verwendet, um Metalle vor der Verarbeitung zu „reinigen“, um Rost, Zunder und andere Verunreinigungen von ihrer Oberfläche zu entfernen.
- Herstellung organischer Verbindungen: Salzsäure wird als Reagens zur Gewinnung von Vinylchlorid verwendet, das bei der Herstellung von Kunststoffen verwendet wird. Salzsäure stammt auch aus Chloropren, das in synthetischen Kautschuken verwendet wird.
- Herstellung anorganischer Verbindungen: Salzsäure kommt in mehreren industriellen Prozessen zur Herstellung von Reagenzien und Verbindungen vor anorganische Stoffe, darunter Produkte zur Wasseraufbereitung, wie Eisen(III)-chlorid und Aluminium.
- Als Reinigungsmittel verwendet: Salzsäure wird auch als Salzsäure vermarktet und wird für die Bau-, Haushalts- und chemische Reinigung von Werkzeugen und Maschinen verwendet.
- Lebensmittelverarbeitung: Salzsäure wird in verschiedenen Reaktionen zur Herstellung von Nahrungsmitteln und Zusatzstoffen verwendet, beispielsweise bei der Hydrolyse von Stärke und Proteinen, oder im Endprodukt zum pH-Gleichgewicht.
- Arzneimittelherstellung: Salzsäure wird bei der Herstellung von löslichen Hydrochloriden verwendet, die in mehreren Arzneimitteln enthalten sind, wie z. B. Doxycyclinhydrochlorid, das bei der Behandlung von Typhus-Fieber und Pocken.
Salzsäure im Körper
Salzsäure ist in unserem Verdauungssystem, der von unserem Magen produzierte Magensaft ist eine Lösung aus Wasser, Enzymen, Salzsäure, anorganischen Salzen und einem kleinen Prozentsatz Milchsäure.
Ö Speisekuchen wird in Chymus verwandelt, eine saure Masse (dank der Wirkung des Magensaftes und seiner sauren Zusammensetzung), dann ist die Verdauung von Proteine, umgewandelt in Polypeptide und Aminosäuren das wird vom Körper aufgenommen.
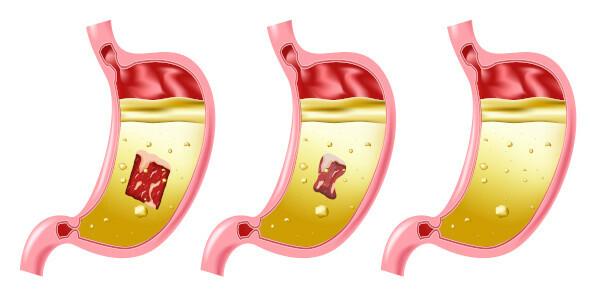
Gefahren durch Salzsäure
Salzsäure ist eine sehr starke und ätzende Säure, daher verursacht der Kontakt mit dem Stoff mehrere Schäden:
- Haut: Verursacht Verätzungen und Reizungen.
- Augen: Verursacht schwere Reizung und kann zur Erblindung führen.
- Inhalation: Verursacht Reizungen und Verletzungen der oberen Atemwege.
- Einnahme: Verursacht Verätzungen im gesamten Mundsystem und im Magen-Darm-Trakt kann es zu Erbrechen, Blutungen, Durchfall und Kreislaufproblemen kommen, die zum Tod führen können.
- Expositionfortgesetzt werden: greift zuerst die Schleimhautbereiche an und verursacht Dermatitis und Bindehautentzündung, Zahnfleischbluten, Photosensibilisierung; Häufiges Einatmen, auch in geringen Konzentrationen der Verbindung, kann zu Gastritis und Nasenbluten.
Auch zugreifen: Eigenschaften und Eigenschaften von Essigsäure

gelöste Übungen
Frage 1 - (Udesc) Bezüglich Salzsäure kann festgehalten werden:
A) in wässriger Lösung ermöglicht es den Durchgang von elektrischem Strom.
B) ist eine Disäure.
C) ist eine schwache Säure.
D) hat einen geringen Ionisierungsgrad.
E) ist eine ionische Substanz.
Auflösung
Alternative A. Salzsäure ist keine Disäure, da sie nur ein ionisierbares H besitzt, aber ein starke Säure, molekulare Substanz mit hohem Ionisationspotential. DAS Ionisation in wässrigem Medium fördert die Leitung von elektrischer Strom aufgrund der Existenz freier Ionen.
Frage 2 - In einer Lösung von Salzsäure und Wasser können wir sagen, dass das Auftreten von molekularem Chlorwasserstoff (HCl) minimal ist, weil
A) Salzsäure in Kontakt mit Wasser wird verdünnt.
B) Chlorwasserstoff ist eine Substanz, die in Wasser nicht löslich ist.
C) Chlorwasserstoff hat ein hohes Ionisationspotential, daher bildet das HCl-Molekül in wässrigem Medium H-Ionen+ Cl-.
D) die Salzsäure, die sehr flüchtig ist, trennt sich von der Lösung und hinterlässt nur Wassermoleküle.
E) Salzsäure ist eine ionische Substanz, daher dissoziiert sie in wässriger Lösung unter Bildung von Ionen.
Auflösung
Alternative C.
A) Die Antwort stimmt nicht mit der Frage überein, das Verdünnen von Salzsäure in Wasser rechtfertigt nicht die Abwesenheit von molekularer HCl.
B) Falsch, Chlorwasserstoff ist löslich und hat eine Affinität zu Wasser.
C) Richtig
D) Obwohl Salzsäure flüchtig ist, tritt diese Entmischung der beiden Spezies in der Lösung nicht signifikant auf.
E) Salzsäure ist eine Lösung aus Chlorwasserstoff und Wasser, wobei Chlorwasserstoff eine nichtionische molekulare Substanz ist.
Von Laysa Bernardes Marques de Araujo
Chemielehrer
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
ARAúJO, Laysa Bernardes Marques de. "Salzsäure"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/Acido-cloridrico.htm. Zugriff am 27. Juni 2021.



