O principgiverusikkerhed, også kaldet Heisenberg usikkerhedsprincippet, blev først anført i 1927, af den tyske fysiker WernerHeisenberg (1901-1976). Dette princip indikerer, at det ikke er muligt at måle, samtidigt og med nøjagtighed, direkte relaterede mængder, f.eks hastighed og position af et legeme.
Seogså: Aspekter af kvanteteori
Usikkerhedsprincippet
Usikkerhedsprincippet vedrører to størrelser, såsom position og momentum eller energi og tid, gennem produktet af usikkerheden ved de målinger, der udføres på dem.
Ifølge usikkerhedsprincippet er jo mere nøjagtig et legems position, jo mindre nøjagtigt måles dets momentum.
Usikkerhedsprincippet siger, at det er umuligt for os med fuldstændig præcision og samtidig at kende to relaterede fysiske størrelser, også kaldet kanonisk konjugerede størrelser.
Hvad er Heisenberg Usikkerhedsprincippet?
O Heisenbergs usikkerhedsprincip er et mærkeligt teoretisk resultat opnået ved beregninger inden for Kvantemekanik, hvis grundlag er netop dette princip. Gennem kendskab til klassisk fysik blev det antaget, at, at kende startposition og hastighed, mere specifikt mængden af bevægelse, af et legeme eller et legemsystem, ville det være muligt at forudsige dets adfærd i fremtidige øjeblikke. På denne måde ville det være muligt at beregne
positioner senere at bestemme dens bane, værdier af acceleration,hastighed,energi, etc. Usikkerhedsprincippet viser imidlertid, at selvom vi havde merenødvendig af måleinstrumenterne ved hånden, ville det ikke være muligt for os at vide, samtidigt og med nøjagtighed, storhed som position og beløbetibevægelse ellerenergi og pauseitid af samme krop.Seogså: Mængde af bevægelse
Så ifølge dette princip, hvis vi kan bestemme position af et legeme med total præcision, vil vi helt miste målene for dets beløbetibevægelse, da upræcisionen om det vil blive betragtet som uendelig. Ligeledes, hvis vi kan være sikre på bevægelsen af et legeme, vil det ikke være muligt at kende dets position.
Det samme gælder for de store energi og tid: hvis vi ved nøjagtigt mængden af energi i en partikel, mister vi præcision i tidsmålinger. Ligeledes, hvis vi ved, hvor lang tid det tog for en begivenhed at forekomme med en bestemt partikel, ville vi helt miste information om mængden af energi til stede i den.

På grund af usikkerhedsprincippet er det umuligt for et legems laveste energiniveau at være nul.
Seogså: Hvad er energi?
Ikke alle fysiske størrelser er relateret til hinanden for deres grad af præcision. Det er f.eks. Muligt at bestemme energi og position af en partikel uden at præcisionen af disse målinger er omvendtproportional hinanden.
Stop ikke nu... Der er mere efter reklamen;)
Desuden pålægger usikkerhedsprincippet, at produktet af usikkerheden af to størrelser, såsom position og momentum, altid vil være større end eller lig med Planck er konstant (h) divideret med 4π. Det er dog almindeligt at se ligningen af usikkerhedsprincippet skrevet med hensyn til Plancks konstant reduceret (? = h / 2π).
Heisenbergs usikkerhedsprincip, som vedrører usikkerhedgiverposition af et legeme med usikkerhed om dens momentum, er defineret gennem ligningen nedenfor:
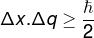
Δx - positionssikkerhed (m)
q - usikkerhed om momentum (m / s)
? - reduceret Planck-konstant (1.0545.10−34 J.s)
Usikkerhedsprincippet anvendes også på kroppens energi og tidsrum. Holde øje:

ΔAnd usikkerhed i energi (J)
t usikkerhed i tid (er)
Antag for eksempel, at du i et givet eksperiment vil måle position af en elektron. For at kunne måle sin position er det nødvendigt, at der på en eller anden måde udsendes en foton mod denne elektron. Men når foton reflekteres tilbage til observatøren, elektronen rekylerer, da fotonet overfører en lille mængde bevægelse direkte til den frekvens. Hvis vi mere nøjagtigt vil bestemme placeringen af denne elektron, kan vi øge fotonets frekvens. Men hvis vi gør dette, vil vi øge mængden af bevægelse givet til elektronen og dermed miste præcisionen ved måling af denne størrelse.
Seogså: Hvad er strengteori?
Løst øvelse på usikkerhedsprincippet
En ekstremt nøjagtig laboratoriemåling er i stand til at bestemme placeringen af et molekyle med måleusikkerhed af rækkefølge lig med ± 10-15 m. I henhold til usikkerhedsprincippet, hvad er den mindste mulige usikkerhed ved måling af momentet i dette molekyle?
Løsning
Usikkerhedsprincippet siger, at produktet af positionen og momentumusikkerheden skal være større end eller lig med halvdelen af den reducerede Planck-konstant:

Således tager modulus af positionsusikkerheden (Δx = 10-15) leveret af øvelsen og det reducerede Planck-konstantmodul (? = 1,0545.10−34 J.s), bliver vi nødt til at:

Resultatet ovenfor indikerer, at selvom laboratoriet har et instrument, der er i stand til at måle bevægelsesmængden for denne partikel med mindre fejl end 10-20 m, vil det ikke være muligt at måle dens værdi nøjagtigt. Så vi har altid værdien beregnet ovenfor som en plus eller minus afvigelse.
Af mig Rafael Helerbrock


