Polymerisering er navnet på den kemiske proces, der resulterer i dannelsen af makromolekyler (store molekyler) kaldet polymerer gennem kombinationen af mindre molekyler, monomererne.
reaktionen af polymerisering det er meget almindeligt i naturen, som vi kan se i kulhydrater (som stivelse) og proteiner (som kasein i mælk). Det forekommer også syntetisk, da langt størstedelen af polymerer, der anvendes af mennesker i deres daglige liv, er fremstillet kunstigt.
Den første polymer fremstillet af polymerisering syntetisk var bakelit i 1909 af den belgiske kemiker Leo Hendrik Baekeland.
Generelt skal en monomer kombineres med en anden (uanset om de er ens eller forskellige) i en reaktion af polymerisering, er det nødvendigt eksistensen af fri valens (kemisk binding, der skal udføres) i begge monomerer.
Disse valenser opstår som et resultat af brydningen af bindinger ved anvendelse af katalysatorer (såsom nikkel), eksterne forhold såsom lys og varme eller ved fænomenet resonans i strukturen (skift af elektroner).
Ved dannelsen af polypropylen (PP-polymer), f.eks. Anvendt i husholdningsredskaber og legetøj, er det pi-link (π) i hvert molekyle er opdelt som følger:
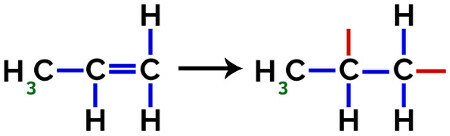
Brud på pi-binding i propylen
Således kan hver propylenmonomer binde sig til to andre propylenmonomerer og danne polymeren PP eller polypropylen (præfikset poly indikerer flere monomere enheder). Den hyppigste måde at repræsentere en polymer på er monomeren mellem parenteser og på ydersiden bogstavet n, som angiver flere monomerer, som vi kan se i tilfældet med PP-polymeren:
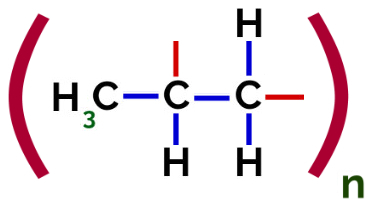
Repræsentation af PP-polymer
reaktionen af polymerisering kan gøres på forskellige måder, som vi vil se nedenfor:
a) Reaktion af yderligere polymerisering
Heri polymerisering, er der altid et brud på en pi-binding i monomeren, som får to frie valenser til at vises i strukturen, som i dannelsen af polyethylen, polymer, der er meget anvendt i farmaceutisk emballage.
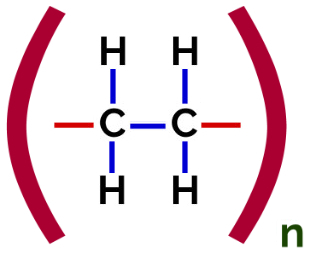
Polyethylen Addition Polymer Structural Formula
På polymerisering af polyethylen anvendes molekyler af ethylen (ethen) som monomeren, som har en pi-binding mellem de to carbonatomer. Når denne binding brydes, vises to frie valenser, en på hvert carbonatom, der var involveret i pi-bindingen. Monomererne forener sig nøjagtigt i hver af disse valenser, det vil sige at den ene valens er knyttet til den andens valens og så videre.
Stop ikke nu... Der er mere efter reklamen;)
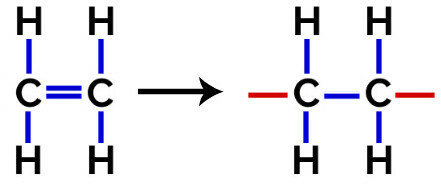
Ligning af polyethylendannelse
b) Additionspolymerisationsreaktion 1.4
I denne polymerisation præsenterer monomererne to alternerende dobbeltbindinger (en pi og en sigma), hvilket favoriserer fænomenet af resonans (skiftevis placeringen af pi-elektronerne i pi-bindingen) som ved dannelsen af syntetisk gummi (polybutadien)

Strukturel formel for polybutadien
Den monomere enhed af denne polymer er butadien, som har to alternerende dobbeltbindinger. Med resonans har strukturen en dobbeltbinding mellem kulstof 2 og 3 og to frie valenser på kulstof 1 og 4. Det er netop i disse frie valenser af carbon 1 og 4, at monomererne kombineres.

Resonans i butadien
c) Reaktion af kondensationspolymerisation eller eliminering
Det er en reaktion af polymerisering hvor obligatorisk to monomerer (de samme eller forskellige) samtidigt mister atomer eller grupper, hvilket resulterer i to frie valenser i hver enkelt af dem. På denne måde er der altid eliminering af hydrogen fra en monomer, som derefter forbinder et halogen (F, Cl, Br, I), OH, NH2eller til CN for den anden monomer.
Så i polymerisering ved eliminering er der altid dannelse af vand, halogeneret syre (HCI, HI, HF, HBr), ammoniak (NH3) eller hydrocyansyre (HCN) ud over polymeren. Se for eksempel repræsentationen af dannelsen af polyester, et materiale der bruges som stof:

Polyesterformationsligning
Polyesterdannende monomerer er p-benzensyre og ethan-1,2-diol. Det kan vi se i dette polymerisering eliminering af vandmolekyler sker, da de to monomerer har to hydroxyler. I denne proces mister syren de to hydroxyler, og dialkoholen mister kun brint fra dens hydroxyler:

Polyester struktur
Polyestermonomerer er forbundet med ilt i alkoholen og kulstof i carboxylsyren.
Af mig Diogo Lopes Dias


