Валентният слой е последният слой от електронното разпределение на атома. Тъй като това е най-външният слой, той е и най-отдалечен от атомното ядро.
Според Правило за октет, валентната обвивка се нуждае от осем електрона, за да се стабилизира.
По този начин атомите придобиват стабилност, когато имат 8 електрона във валентната обвивка. Това се случва с благородни газове, те имат пълния валентен слой. Единственото изключение е елементът хелий, който има 2 електрона.
Останалите елементи трябва да създадат химически връзки, за да получат липсващите електрони и да достигнат осемте електрона във валентната обвивка.
Електроните на валентната обвивка са тези, които участват в връзките, тъй като те са най-външните.
Електросферни слоеве
Според атомния модел на Ръдърфорд-Бор електроните се въртят около атомното ядро в различни енергийни слоеве.
Има седем слоя, обозначени с буквите K, L, M, N, O, P и Q. Всеки поддържа максимален брой електрони.
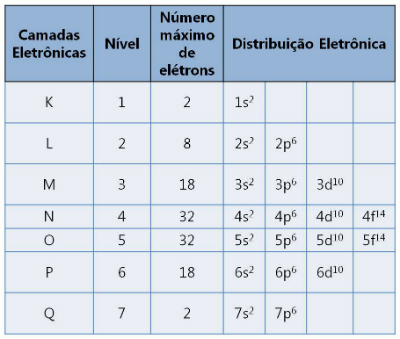 Електронни слоеве и броя на електроните, които те поддържат
Електронни слоеве и броя на електроните, които те поддържат
Прочетете също:
- Атомният модел на Бор
- Атомният модел на Ръдърфорд
- Благородни газове
- Правило за октет
Как да определите слоя Валенсия?
Валентният слой може да се определи по два начина: Eletronic разпространение и Периодичната таблица.
За да се определи валентният слой чрез електронно разпределение, Диаграма на Линус Полинг.
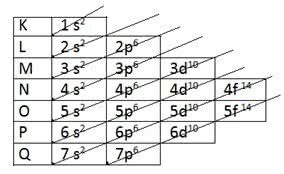 Диаграма на Полинг
Диаграма на Полинг
Припомнете си, че диаграмата на Полинг следва нарастващия ред на енергията. Последният слой, получен при електронното разпределение, е валентният слой.
1s2 2 секунди2 2р6 3 секунди2 3p6 4s2 3d10 4р6 5s2 4г10 5p6 6s2 4f14 5 д10 6p6 7s2 5е14 6г10 7p6
И така, във валентния слой най-енергийният подниво е последният слой.
Примери:
Азот - N
Атомен номер: 7
Електронно разпространение: 1s2 2 секунди2 2р3
Валенсия слой: 2s2 2р3, N има 5 електрона във валентната обвивка.
Желязо - Fe
Атомен номер: 26
Електронно разпространение: 1s2 2 секунди2 2р6 3 секунди2 3p6 4s2 3d6
Валенсия слой: 4s2, Fe има 2 електрона във валентната обвивка.
Хлор - Cl
Атомен номер: 17
Електронно разпространение: 1s2 2 секунди2 2р6 3 секунди2 3p5
Валенсия слой: 3 секунди2 3p5, Cl има 7 електрона във валентната обвивка.
Кислород - O
Атомен номер: 8
Електронно разпространение: 1s2 2 секунди2 2р4
Валенсия слой: 2s2 2р4, кислородът има 6 електрона във валентната обвивка.
Въглерод - С
Атомен номер: 6
Електронно разпространение: 1s2 2 секунди2 2р2
Валенсия слой: 2s2 2р2, въглеродът има 4 електрона във валентната обвивка.
Прочетете и за Квантови числа.
Досега използваните примери са с елементи на основно състояние. Но същият принцип може да се използва за йони, катиони и аниони. Вижте примера:
Хлорид анион - Cl-
Атомният номер на хлора е 17. Ако беше в основно състояние, броят на електроните щеше да бъде равен на броя на протоните. В този случай обаче има печалба от 1 електрон.
Първо направете електронното разпределение на хлорния елемент:
1s2 2 секунди2 2р6 3 секунди2 3p5
С печалбата на допълнителен електрон, добавете в последния слой:
1s2 2 секунди2 2р6 3 секунди2 3p6. Така че има 8 електрона във валентната обвивка (3s2 3p6).
Вижте също: Упражнения по електронно разпространение.
За да се определи валентният слой чрез периодичната таблица, е необходимо да се идентифицират периодът и семейството на елементите.
По този начин, докато 1А семейство има 1 валентен електрон, 2А има 2 и т.н. Химичните елементи, съдържащи се в него семейство на периодичната таблица имат еднакъв брой електрони във валентната обвивка.
Това обаче е валидно само за групи 1, 2, 13, 14, 15, 16 и 17, които имат следния брой електрони във валентната обвивка съответно 1, 2, 3, 4, 5, 6 и 7.
За елементи, при които тази връзка не е възможна, трябва да се използва електронно разпространение.
Не забравяй! В химически връзки възникват от необходимостта да се стабилизират атомите и по този начин да се образуват молекули. Това става чрез даряване на електрони от валентната обвивка, които, тъй като са по-далеч от ядрото, имат тенденция да даряват.
Прочетете и за Молекулярна геометрия.
Упражнения
1. Намерете валентния слой на следните елементи:
Бром
35бр
1s2 2 секунди2 2р6 3 секунди2 3p6 4s2 3d10 4р5
Бромната валентна обвивка (семейство 7А) има 7 електрона. Това е така, защото 4s2 и 4р5 принадлежат на N слоя, докато 3d10 принадлежи към слой М.
Алуминий
13Ал
1s2 2 секунди2 2р6 3 секунди2 3p1
Алуминиевата валентна обвивка (семейство 3А) има 3 електрона.
2. (UFSC) Броят на електроните във всяко подниво на стронциевия атом (38Sr) във възходящ ред на енергията е:
а) 1s2 2 секунди2 2р6 3 секунди2 3p6 4s2 3d10 4р6 5s2
б) 1s2 2 секунди2 2р6 3 секунди2 3p6 4s2 4р6 3d10 5s2
в) 1s2 2 секунди2 2р6 3 секунди2 3p6 3d10 4s2 4р6 5s2
г) 1s2 2 секунди2 2р6 3 секунди2 3p6 4р6 4s2 3d10 5s2
д) 1s2 2 секунди2 2р6 3p6 3 секунди2 4s2 4р6 3d10 5s2
а) 1s2 2 секунди2 2р6 3 секунди2 3p6 4s2 3d10 4р6 5s2
3. (IFSP / 2013) Броят на електроните във валентната обвивка на калциевия атом (Z = 20), в основно състояние, е
до 1
б) 2
в) 6
г) 8
д) 10
б) 2
Проверете въпросите за приемния изпит с коментирана резолюция в: Упражнения върху периодичната таблица.