НА молекулярна геометрия, тоест разположението на атомите на молекулата, може да се определи от правилото на химика Gillespie, в който той изброява броя на атомите, прикрепени към централен атом, и броя на облаците електроника.
Знанието за геометрията на молекулата е изключително важно, защото ни помага определят полярността и, следователно, разтворимостта (съгласно правилото за подобни разтваря подобен).
с обаждането тетраедрична геометрия, не е по-различно. Вижте критериите за определянето му съгласно правилата на Gillespie:
Пентатомични молекули (пет атома);
Липса на електронни облаци в централния атом;
композитни молекули или съставни аниони.
Някои примери за молекули, чиято геометрия е тетраедрична те са:
CH4

СН структурна формула4
Въглеродът има четири електрона във валентната си обвивка и всички тези електрони се свързват с водород. Ето защо въглеродът няма електронен облак (допълнителна двойка електрони).
САМО4-2
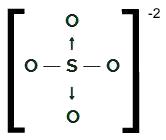
Структурна формула на ОС4-2
Сярата, която има шест електрона във валентната обвивка, прави две единични връзки с два кислородни атома и два
дативни ковалентни връзки с другите два кислорода. В единични връзки той използва два от своите електрони и във всеки датив използва други два (общо четири електрона, участващи в датите), общо шест електрона. Като такъв не е останал облак.NH4+

NH структурна формула4+
Азотът, който има пет електрона във валентната обвивка, прави три единични връзки с водородните атоми и дативна връзка с другия водород. В единични връзки той използва три от своите електрони, а в дативните използва още два, общо пет електрона. Като такъв не е останал облак.
CH3Cl
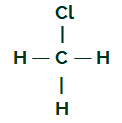
СН структурна формула3Cl
Не спирайте сега... Има още след рекламата;)
Въглеродът има четири електрона във валентната си обвивка и всички тези електрони се свързват с водородите и хлорния атом. Поради тази причина въглеродът няма електронен облак.
→ Полярност на молекулата
Знаейки, че дадена молекула има тетраедрична геометрия, можем да определим нейната полярност изключително проста форма, тъй като молекулата заема своите четири полюса (четири лиганда в атома централен). За това е достатъчно да знаете характеристиките на свързващите вещества и да вземете предвид едно от следните правила:
Ако броят на облаците е равен на броя на равни лиганди = неполярна молекула;
Ако броят на облаците е различен от броя на равни лиганди = полярна молекула.
В следните две молекули, чиято геометрия е тетраедрична, можем да приложим правилата по-горе и да посочим тяхната полярност:
Молекула на метан
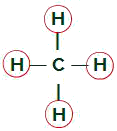
Равни лиганди в молекулата на метана
Молекулата на метана има четири електронни облака (четири единични връзки), а също и четири водородни атома, прикрепени към централния атом. Поради това, ние имамечетириоблаци и четири еднакви свързващи вещества, скоро, молекулата е неполярна.
Наблюдение: Ако молекулата на веществото е аполат, той се разтваря добре в друго вещество, чиито молекули също са неполярна.
Молекула на хлорометан

Равни лиганди в молекулата на хлорометана
Молекулата хлорометан има четири електронни облака (четири единични връзки) и три водородни атома и един хлорен атом, прикрепен към централния атом. Поради това, ние имамечетириоблаци и три равни лиганди (три водорода); скоро, молекулата е полярна.
Наблюдение: Ако молекулата на веществото е полярен, той се разтваря добре в друго вещество, чиито молекули също са полярна.
От мен Диого Лопес Диас
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
ДНИ, Диого Лопес. „Тетраедрична геометрия“; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/geometria-tetraedrica.htm. Достъп на 28 юни 2021 г.


